物質が結晶化する理由
* 強い分子間力: 強い分子間力(水素結合、双極子型相互作用、ロンドン分散力など)を持つ物質は、固体状態で順序付けられた配置を支持する傾向があります。これらの力は、通常の繰り返しパターンで分子またはイオンを一緒に保持し、結晶格子をもたらします。
* 通常の形状と対称性: 比較的規則的で対称的な形状を持つ分子またはイオンは、より効率的に繰り返し構造に詰まることができます。これが、多くのイオン化合物(NaClなど)といくつかの有機分子(糖など)が結晶を形成する理由です。
* ゆっくりした冷却: 液体または溶液がゆっくりと冷却されると、分子は自分自身を整列させ、結晶化に必要な順序付けられた配置を形成する時間を増やします。迅速な冷却は、結晶性固体ではなく、アモルファスソリッド(ガラス状)につながる可能性があります。
一部の物質が結晶化しない理由
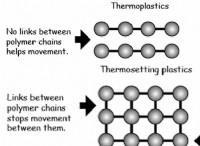
* 分子間力の弱い: 分子間力が弱い物質には、ランダム性を克服し、高度に秩序化した結晶構造を形成するのに十分なエネルギーがない場合があります。これらの物質はしばしばアモルファス固体(ポリマー、ガラスなど)を形成します。
* 複雑な分子構造: 不規則または複雑な形状の分子は、繰り返しパターンに効率的に梱包することが困難になる可能性があります。
* 不純物: 溶液中の不純物は、通常の結晶格子の形成を混乱させる可能性があります。
* 迅速な冷却: 溶液があまりにも速く冷却された場合、分子は結晶格子に自分自身を並べる時間がありません。
例
* 結晶固体: 塩(NaCl)、砂糖(スクロース)、氷(H2O)
* アモルファス固体: ガラス、ゴム、プラスチック
覚えておくべきキーポイント:
* 結晶化は、順序付けられた配置のプロセスです。
* 分子間力とより単純な分子構造が結晶化を好む。
* 冷却速度と不純物の存在は、結晶化に影響を与える可能性があります。
これらの要因のいずれかをより詳細に調査したい場合は、具体的な例を念頭に置いてください。