その理由は次のとおりです。
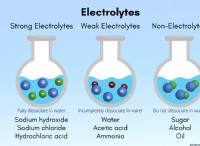
* 珪藻原子 同じ元素の2つの原子が電子を共有して、安定した電子構成を実現するときに形成されます。この共有は共有結合を作成します。例には、o₂(酸素)、n₂(窒素)、およびH₂(水素)が含まれます。
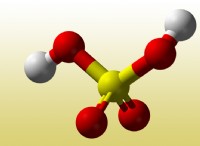
* 多原子イオン 異なる元素の複数の原子が電子を共有すると形成され、正味の正または負の電荷が生じます。これらの共有電子も共有結合を形成します。例には、so₄²⁻(硫酸塩)、no₃⁻(硝酸塩)、およびnh₄⁺(アンモニウム)が含まれます。
共有結合に関する重要なポイント:
* 電子の共有: 共有結合には、原子間の電子の共有が含まれます。
* 非金属原子: 共有結合は通常、非金属原子間で発生します。
* 強い債券: 共有結合は一般的に強力であり、壊れるのにかなりのエネルギーが必要です。
* 分子構造: 共有結合は分子の形成をもたらし、これは共有結合によって結合された原子の明確な単位です。
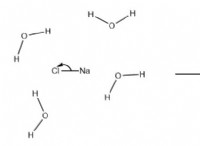
イオン結合は化合物の形成にも重要ですが、それらは主に電子の共有ではなく、原子間の電子の伝達を含みます。