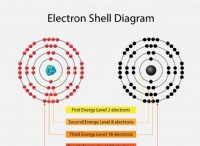
* 酸素の電子構成: 酸素には8つの電子があります。その電子構成は1S²2S²2P⁴です。 これは、6つの原子価電子(最も外側のシェルに電子)があり、安定したオクテット(外殻に8電子)を実現するためにさらに2つ必要です。
* 共有結合: 酸素は、別の酸素原子と二重共有結合を形成することにより安定性を達成します。共有結合では、原子は電子を共有して外側の殻を満たします。
* 2つのペアの共有: 酸素分子(O₂)では、各酸素原子は2つの電子を結合に寄与します。これにより、共有電子が2つのペアが形成されます。
* ダブルボンド: 2組の電子を共有すると、二重結合が作成されます。この二重結合は強く、酸素原子を一緒に保持します。
鍵は、酸素原子が4つの総電子ではなく、2組の電子を共有することです。この共有は二重結合をもたらします。これは、両方の酸素原子が安定したオクテットを達成するために必要です。