VSEPRモデルに基づくCCL4およびNH3の極性に関する仮説:
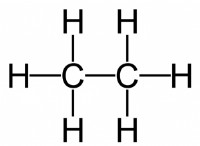
ccl4:
* vSEPRモデル: CCL4の中心炭素原子は、四面体配置(AX4)の4つの塩素原子に囲まれています。
* 極性仮説: 四面体の形状と炭素と塩素の類似の電気陰性度により、個々のC-CL結合双極子は互いにキャンセルします。これにより、非極性分子が生じます 。
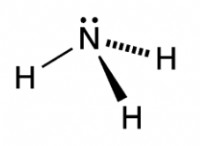
nh3:
* vSEPRモデル: NH3の中心窒素原子は、三角錐体配置(AX3E)の3つの水素原子と1つの孤立した電子のペアに囲まれています。
* 極性仮説: N-H結合は、窒素の電気陰性度が高いため極性です。窒素上の唯一のペアは、分子の全体的な非対称性に寄与します。これらの要因により、極地分子が生じます 正味の双極子モーメントが窒素原子を指しています。
要約:
* ccl4 非極性であると予測されています 対称性四面体の幾何学と結合双極子のキャンセルにより。
* nh3 極性であると予測されています 非対称の三角錐体幾何学と窒素上の孤立ペアの存在により、純双極子モーメントが生じます。
注: これは、VSEPRモデルに基づく仮説です。極性を確認するには、実験的証拠が必要です。