周期表では、炭素 (C)、ケイ素 (Si)、ゲルマニウム (Ge)、スズ (Sn)、および鉛 (Pb) は、14 族または炭素族のメンバーとして知られています。 p ブロック 、その外部電子配置 ns2np2 は、p 軌道に 2 つの電子のみで見つかります。
第 14 族元素の半径に注意を払うと、第 14 族元素の半径が第 13 族元素の半径よりも小さいことがわかります。これは主に有効核電荷のためです。半径は炭素からシリコンへと増加しますが、主に d 軌道と f 軌道が原因で減少します。
このグループのイオン化エネルギーをグループ 13 のイオン化エネルギーと比較すると、主にその原子のサイズのために、そのイオン化エネルギーが非常に高いことがわかります。また、上から下に行くと、イオン化エンタルピーが減少することがわかっています.
第 14 族の元素は、主に固体構造のため、非常に高い融点と沸点を持っています。 Sn と Pb には 2 つの結合が存在するため、融点が低くなります。炭素は格子構造をしており、その融点は他のすべてのものよりもはるかに高いです。このグループで下に行くほど、融点が低下します。
炭素化合物
炭素に関連する化合物の数は、他のすべての元素から構成される化合物の数よりもはるかに多くなります。炭素は、そのさまざまな特性のために多くの化合物を形成します。メタン (CH4) は、その親化合物として知られています。これとは別に、炭化水素は、水素と炭素の組み合わせによって形成される親化合物としても知られています。これらの化合物の形成には多くの結合も存在し、単結合、二重結合、または三重結合が見られます。
結合の数に基づいて、炭素化合物は 2 つの主要なカテゴリに分類されます。これは、主に飽和炭素化合物と不飽和炭素化合物の間に見られる C 原子間で見られます。これについては、以下で説明します。
飽和炭素化合物 - 飽和炭素化合物は、鎖または環内の異なる炭素原子が単結合のみで結合している炭素化合物です。アルカンは、以下に示すように、飽和鎖とエタンの構造に似た構造を持つ炭素化合物です。
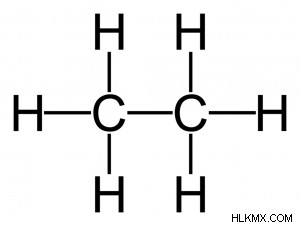
不飽和炭素化合物 - 不飽和炭素化合物には、炭素原子への二重結合または三重結合が含まれており、これらの結合がそれらを鎖または環に結合しています。最も一般的な不飽和鎖炭素化合物は、アルカンとアルキンです。アルカンは主に炭素原子間の二重結合によって結合され、アルキンは炭素原子間の三重結合によって結合されます。以下はエテンの例です。
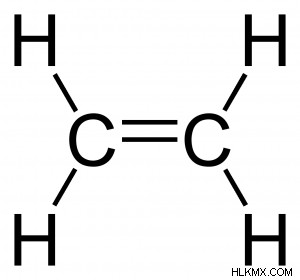
シリコン
シリカやケイ酸塩などの化合物は、地球の地殻の約 95% に含まれています。シリカは主に二酸化ケイ素として知られています。シリカの他の形態には、石英、クリストバライト、トリジマイトなどがあります。シリコは共有結合化合物であり、4 つの酸素原子を持つ四面体です。
シリコーン - シリコーンは、繰り返し単位を含む有機ケイ素ポリマーの構成要素です。アルキル基またはアリール基を置換することによって作られます。非極性のアルキル基で囲まれていることも注目に値します。
ケイ酸塩 - ゼオライトは別のタイプのケイ酸塩で、構造は SiO4 (単一のケイ素原子に結合した 4 つの酸素原子) です。ケイ酸環は、鎖と立体構造の両方を形成できます。
ゼオライト - ゼオライトはかつて、石油化学産業で触媒として利用されることが知られていました。これらはアルコールと結合し、ZSM-5 と呼ばれるゼオライトを使用してガソリンに変換されます。ゼオライトは、硬水を軟化するために最も一般的に使用されます.
ゲルマニウム
このセクションでは、ハロゲンはハロゲン化物、酸素は酸化物、水素は水素化物として説明されています。ここでは、いくつかの二元化合物、追加のゲルマニウム化合物、およびすべての化合物、特に p ブロック要素のゲルマニウム酸化値を示します。酸化数に基づいて、電気的構成も提供されます。酸化数 4、2、および -4 は、ゲルマニウムで最も頻繁に見られます。
水素化物 | 四水素化ゲルマニウム:GeH4 六水素化ジゲルマニウム:Ge2H6 |
フッ化物 | 二フッ化ゲルマニウム:GeF2 四フッ化ゲルマニウム:GeF4 |
塩化物 | 二塩化ゲルマニウム:GeCl2 四塩化ゲルマニウム:GeCl4 |
ヨウ化物 | 二ヨウ化ゲルマニウム:GeI2 四ヨウ化ゲルマニウム:GeI4 |
酸化物 | 酸化ゲルマニウム:GeO 二酸化ゲルマニウム:GeO2 |
すず
スズは、酸化状態 4 のスズに存在する、酸化第二スズとしても知られる SnO2 の酸化スズ (IV) の鉱物形態で見つかります。酸化スズ (II) と酸化第一スズは、SnO の 2 つの形態です。 2 つの酸化状態で存在します。臭化スズ (II) は、SnBr2、塩化スズ (II)、SnCl2、フッ化スズ (II)、SnF2、およびヨウ化スズ (II) としても知られ、酸化状態 2 のスズを含む化合物です。臭化スズ (IV) は SnBr4 で構成され、塩化スズ (IV) は SnCl4 で構成され、フッ化スズ (IV) は SnF4 で構成され、ヨウ化スズ (IV) は SnI4 で構成されます。
結論
14 族の主な元素は、炭素 (C)、シリコン (Si)、ゲルマニウム (Ge)、スズ (Sn)、鉛 (Pb) であり、元素としてだけでなく、化合物として。医療から産業まで幅広い分野で活躍しています。自然界には、これらの成分のいくつかが豊富に存在します。一方、炭素、シリコン、ゲルマニウムは、信じられないほど安定した固体構造のため、非常に高い融解温度と沸点を持っています.