水(H₂O)は極分子です:
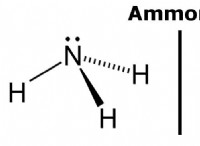
* 極性: 水は、酸素原子のより高い電気陰性度のために曲がった形状であり、酸素に部分的な負電荷と水素の部分的な正電荷を生成します。この不均一な電荷分布は、極性分子になります。
充電および極性分子:
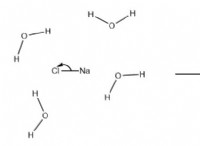
* 帯電した分子: これらの分子には、完全な、永久的な正または負の電荷があります(たとえば、na⁺、cl⁻などのイオン)。
* 極分子: これらの分子には不均一に分布した電荷があり、部分的な陽性および部分的な負電荷の領域(例:エタノール、グルコース)を作成します。
それがどのように機能するか:
1。アトラクション: 極性である水分子は、他の極性または荷電分子の帯電したまたは部分的に帯電した領域と強い静電相互作用(水素結合)を形成します。
2。破壊: これらの魅力は、溶質分子を一緒に保持する力を破壊し、水全体に分離して分散することができます。
3。溶媒和: 水分子は本質的に囲まれ、溶質分子を「溶媒和」し、分散した状態に保ち、それらが組換えを防ぎます。
非極性分子が溶解しない理由:
非極性分子(オイルなど)には均等に分布しています。彼らは水分子との強い相互作用を形成することはできないので、彼らはうまく溶解しません。それらは他の非極性分子と相互作用する可能性が高く、分離につながります。
要約:
荷電および極性分子は、溶質分子を一緒に保持する力を克服するのに十分な強度である水分子と好ましい静電相互作用(水素結合)を形成できるため、水に溶解します。このプロセスは、水中の溶質の分散と溶媒和につながります。