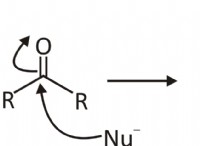
電気陰性度が異なる2つの原子間の共有結合は、電子の不平等な共有と原子の部分的な正電荷と負の電荷の作成をもたらします。
重要な要素の内訳は次のとおりです。
* 共有結合: 2つの原子間の電子ペアの共有によって形成される結合。
* 電気陰性度: 原子が化学結合で自分自身に向かって電子を引き付ける能力。
* 電子の不平等な共有: 原子の電気陰性度は異なるため、共有電子は、より高い電気陰性度のある原子により近い時間を費やします。これにより、より多くの電気陰性原子にわずかな負電荷が生成され、より少ない電気陰性原子にわずかな正電荷が生成されます。
* 部分料金: これらの不均等な電荷は、Δ+(部分陽性)およびΔ-(部分陰性)として表されます。
例: 水分子(H₂O)では、酸素は水素よりも電気陰性です。これにより、酸素原子の部分的な負電荷(Δ-)があり、水素原子には部分的な正電荷(Δ+)がある極性共有結合につながります。
キーテイクアウト: 極性結合結合は分子内に双極子モーメントを作成し、極性にします。この極性は、物質の溶解や水素結合の形成など、多くの生物学的および化学的プロセスにとって重要です。