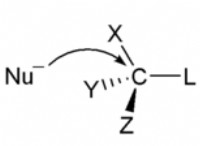
* ナトリウム(Na) 高度に反応性の高いアルカリ金属です。外側の電子を容易に失い、正のイオン(Na+)を形成します。
* エタン酸(CH3COOH) 、酢酸とも呼ばれ、弱酸です。プロトン(H+)を寄付できるカルボキシル基(-COOH)が含まれています。
反応:
ナトリウム金属がエタン酸と接触すると、次の反応が発生します。
2na(s) + 2ch3cooh(aq)→2ch3coona(aq) + h2(g)
* ナトリウム(Na) エタン酸(CH3COOH)と反応します ethanoate(Ch3coona)を形成する および水素ガス(H2) 。
*反応は発熱性であり、熱を放出することを意味します。これにより、混合物が泡立ち、場合によっては慎重に処理されないと水素ガスに火をつける可能性があります。
「中程度」に見える理由:
反応は、ナトリウムと水との激しい反応と比較して「中程度」に見えるかもしれません。これは:
* エタン酸は水よりも弱い酸です。 容易にイオン化しないため、ナトリウムとの反応は遅くなります。
* 反応は局所化されています。 反応はナトリウム金属の表面で発生し、生成された水素ガスは反応を遅くすることができます。
ただし、反応が「中程度」に見えるかもしれないとしても、それは非常に反応性が高く、潜在的に危険であることを覚えておくことが重要です。
安全上の注意事項:
常に注意を払ってナトリウム金属を処理してください。 適切な安全装置と訓練を受けた監督者なしでは、エタン酸にナトリウムを追加しないでください。