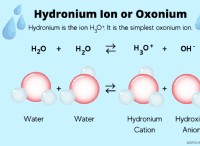
* 酸の強度: 酸強度とは、溶液中の陽子(H⁺イオン)を寄付する酸の傾向を指します。
* 解離: 強い酸はほぼ完全に水で解離(分離)し、高濃度のH孔を放出します。弱い酸は部分的にのみ解離します。
* hcl: 塩酸は強酸です。 水中では、基本的に完全にイオン化して、H⁺イオンとcl⁻イオンを形成します。
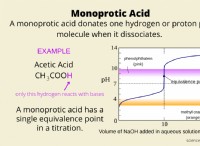
* ch₃cooh: 酢酸は弱酸です。 それは水中で部分的にしかイオン化しません。つまり、HClと比較して多くのh⁺イオンを放出しません。
キーポイント:
* ph: 強酸は、弱酸よりも低いpH(より酸性)を持っています。
* アプリケーション: 酸の強さはその使用を決定します。 HCLは、その強酸性の性質により、多くの産業プロセスに使用されます。 酢酸は酢に含まれており、より穏やかな酸です。