* 塩化鉛(PBCL2) 控えめに溶けやすい塩です。水に溶解すると、鉛(II)イオン(PB²⁺)および塩化物イオン(Cl⁻)に解離します。
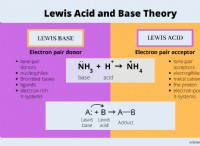
* 水酸化物(OH-) 溶液中にnaohまたはkohのいずれかのように存在できる一般的なベースです。
* 共通イオン効果 溶液にすでに存在するイオンを含む可溶性塩が追加されたときに発生します。 この場合、塩化物イオン(Cl⁻)は、塩化鉛の溶解による溶液にすでに存在しています。
水酸化物イオンの添加は、共通イオンを直接導入しません。水酸化物イオンは鉛イオンと反応して水酸化鉛沈殿物を形成することができますが、これは塩化物イオンの濃度に影響しません。