化合物の色
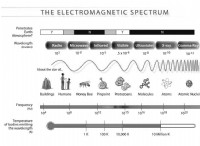
化合物の色は、その電子が光とどのように相互作用するかから生じます。
* 無色の化合物: これらの化合物の電子は光エネルギーを吸収しますが、可視スペクトルには吸収されません。 化合物を通過する光は、変化せずに目に到達し、無色に見えます。
* 色付き化合物: 電子は可視スペクトル内の光を吸収し、その結果、化合物が *吸収されない波長の色を反射または伝達します。
亜鉛と色
亜鉛は遷移金属です しかし、その電子構成はユニークです。 ほとんどの遷移金属とは異なり、亜鉛には完全に満たされたd-oRVITAL があります 。 この充填されたD軌道は、次のことを意味します。
* d-to-D遷移はありません: 遷移金属化合物の色につながる光の吸収は、通常、D軌道の間を移動する電子を伴います。 亜鉛のD軌道はいっぱいであるため、このタイプの遷移は不可能です。
* 亜鉛は無色のイオンを形成します: Zn²⁺イオンは無色です。
* 亜鉛化合物はしばしば無色です: これは、化合物の色が金属イオンによってしばしば決定されるためです。
例:
* 酸化亜鉛(ZNO): 白。 これは、ZnOの広いバンドギャップによるもので、紫外線を吸収することができます。
* 塩化亜鉛(Zncl₂): 無色。
* 硫酸亜鉛(Znso₄): 無色。
例外
* 硫化亜鉛(ZNS): 純粋なときは白ですが、不純物で黄色または茶色に着色することができます。
* クロム酸亜鉛(Zncro₄): 黄色。 これは、本質的に色付けされたクロム酸イオン(クロ²⁻)の存在によるものです。
結論
亜鉛はしばしば無色の化合物を形成しますが、それは保証ではありません。他の要素、特に部分的に満たされたd軌道を持つ要素の存在は、色付きの化合物につながる可能性があります。