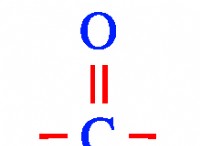* 衝突頻度の増加: 分子がしっかりと詰め込まれると、より頻繁に互いにぶつかります。 分子が十分なエネルギーと衝突すると、新しい結合を壊して形成すると反応が起こります。衝突が多いと、反応が発生する可能性が高くなります。
* 高濃度: 反応物の濃度が高いということは、特定の空間により多くの分子があることを意味し、より頻繁な衝突とより速い反応につながります。
* 表面積: 場合によっては、反応物の表面積も重要です。しっかりと詰め込まれた固形物の表面積が少ない場合がありますが、液体やガスでは、高濃度が依然として衝突の頻度を増加させます。
このように考えてみてください: 混雑したダンスフロアを想像してみてください。より多くの人がいるほど、彼らはお互いにぶつかり、踊り始める可能性が高くなります!
例外:
* フェーズ: 反応物が異なる段階にある場合、いくつかの反応がより速く起こります。たとえば、一方の反応物が液体に溶解し、もう一方の反応物がガスである場合、反応がより速く発生する可能性があります。
* 触媒: 触媒は消費されることなく反応をスピードアップし、反応物をより近くに連れて行くことで作業することがあります。
他に質問がある場合はお知らせください!