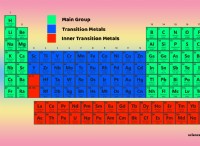
* 電気否定の差: カリウムは金属であり、電気陰性度が低く(0.82)、臭素は高い電気陰性度を持つ非金属です(2.96)。 電気陰性度の違いは大きく(2.14)、1つの要素が電子を獲得し、もう1つの要素がそれらを失う傾向があることを示しています。
* 電子移動: カリウムは、安定した高貴なガス構成を実現するために、単一の原子価電子を容易に失います。一方、臭素は電子を獲得してオクテットを完成させ、臭化イオン(BR-)になります。
* イオンの形成: カリウムは電子を失い、積極的に帯電したカリウムイオン(K+)を形成します。臭素は電子を獲得して、負に帯電した臭化物イオン(BR-)を形成します。
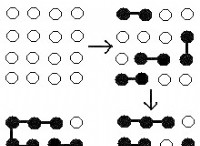
* 静電引力: 反対に帯電したイオン(K+およびBr-)は、静電力を通して互いに引き付けられ、イオン結合を形成します。
これにより、白い結晶性イオン化合物である臭化カリウム(KBR)が形成されます。