鉱酸 水中で解離して水素イオン (H またはプロトン) と共役塩基を生成する無機酸です。グループには多くの有用なベンチ酸が含まれているため、鉱酸は化学および産業において重要です。また、これらの酸の多くは、有機化学物質と無機化学物質の両方を製造するための原料として機能します.
ミネラル酸リスト
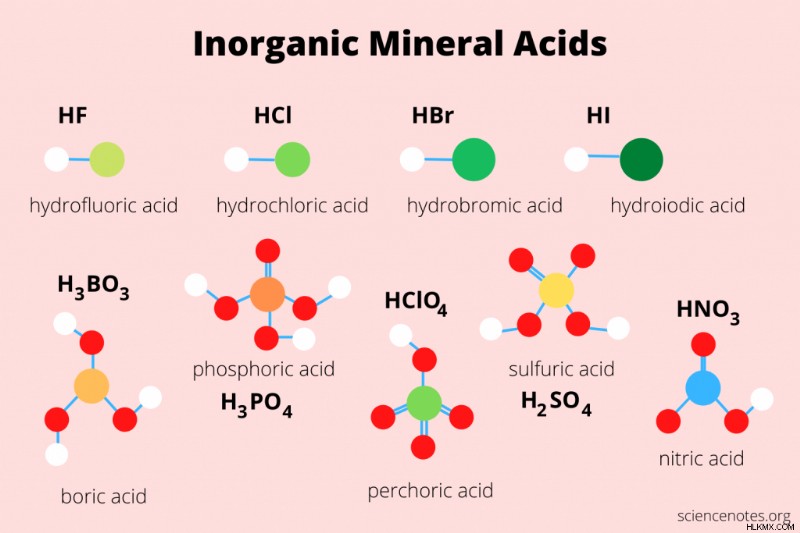
無機酸は、非常に弱い酸 (ホウ酸) から超酸 (過塩素酸) までの範囲です。一塩基性 (塩酸) の酸もあれば、二塩基性 (硫酸) または三塩基性 (ホウ酸) の酸もあります。鉱酸のリストは次のとおりです:
- 王水(塩酸と硝酸の混合物)
- ホウ酸 (H3 BO3 )
- 臭化水素酸 (HBr)
- 塩酸 (HCl)
- フッ化水素酸 (HF)
- ヨウ化水素酸 (HI)
- 硝酸 (HNO3 )
- 過塩素酸 (HClO4 )
- リン酸 (H3 PO4 )
- 硫酸 (H2 SO4 )
- キセン酸 (H2 XeO4 )
ミネラル酸の特性
鉱酸の 2 つの注目すべき特性は、溶解性と腐食性です。鉱酸は水に溶けやすい傾向がありますが、有機溶媒には溶けません。それらは非常に腐食性があります。
無機酸とは対照的に、有機酸であるか、水素を生成しない他の酸があります.ほとんどの場合、ミネラル酸は式に水素が含まれているが炭素がないことで識別できます.たとえば、フルボ酸 (C135 H182 O95 N5 S2 ) は、土壌由来ではありますが、鉱酸ではなく有機酸です。これは、フルボ酸が土壌の有機部分 (腐植質) に由来し、炭素を含み、解離して水素カチオンを生成するためです.
鉱酸の見分け方
鉱酸は化学構造に炭素がなく、腐食性があります。水中で解離すると水素を放出します。ほとんどの鉱酸は有機溶媒に溶解しません.
酢酸は鉱酸ですか?
酢酸 (CH3 COOH) は鉱酸ではありません。炭素を含んでいるので、有機酸です。
参考文献
- Bell, R. P. (1973). 化学における陽子 (第 2 版)。ニューヨーク州イサカ:コーネル大学出版局
- ボイド、クロード E. (2020)。 "酸度"。 水質 :215–231。 doi:10.1007/978-3-030-23335-8_11
- Zumdahl, Steven S. (2009). 化学原理 (第6版)。ホートン・ミフリン・カンパニー。 ISBN 978-0-618-94690-7.