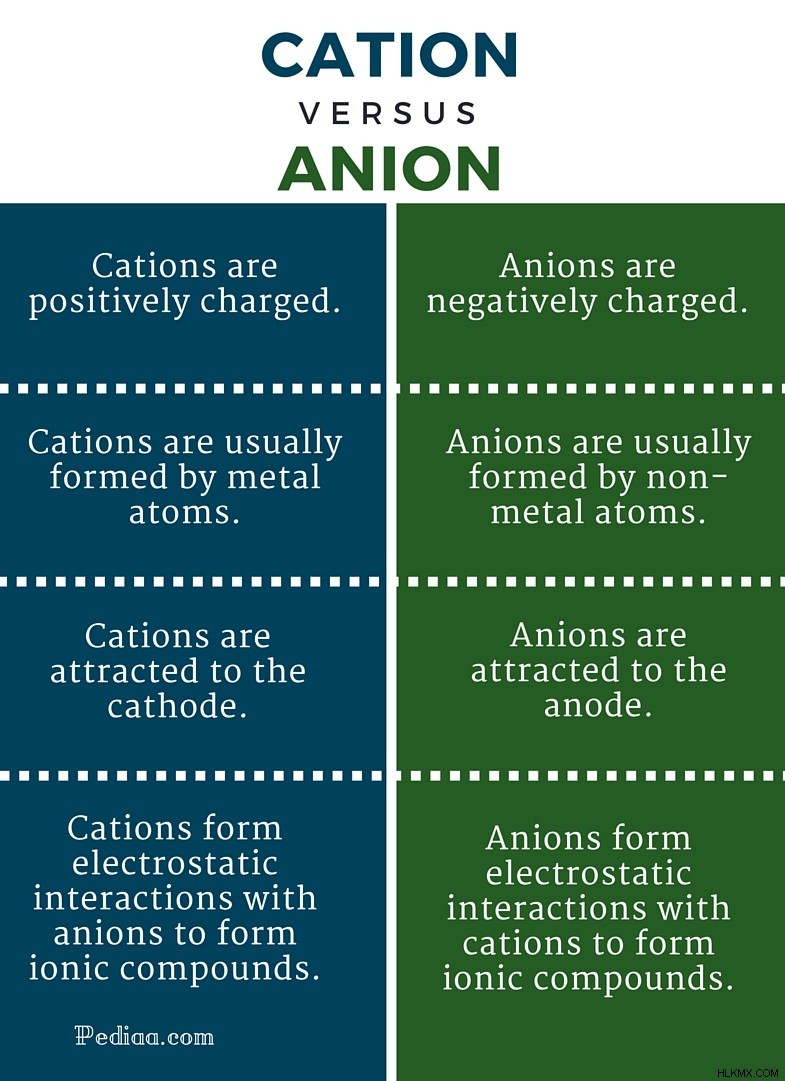
主な違い – 陽イオンと陰イオン
陽イオンと陰イオンは、化学において反対の用語であり、形成される 2 つの主なタイプのイオンを表します。イオンは、実際の状態と比較して、電子が失われたり獲得されたりした状態です。要素が元の形のままである場合、それらは「原子」として知られています。ただし、ほとんどの元素は自然界では原子状態のままではありません。それらは、希ガスのような安定性を達成するために、電子を獲得または放出する傾向があります。化合物形成の前段階として、これらの原子は化合物を「陽イオン」または「陰イオン」と呼ばれる物質の位置または状態に変換します。陽イオンは、原子が電子を放出するときに形成されます。原子が電子を獲得すると陰イオンが形成されます .これが主な違いです 陽イオンと陰イオンの間。
陽イオンとは
前述のように、原子が電子を放出すると陽イオンが形成されます。原子核は、正に帯電した陽子で構成されています。原子は、元の形では、同じ数の電子と陽子を持っています。電子は負に帯電しており、陽子に似た電荷を持っています。したがって、原子が電子を放出すると、原子核内の陽子の数が殻内の電子の数を超えるため、相対的な正電荷が発生します。したがって、陽イオンは正に帯電しています。
通常、陽イオンは、希ガス配置を得ようとして金属原子によって形成されます。ギリシャ語で陽イオンという言葉は「ダウン」を意味し、電子数の低下に関連している可能性があります。電気分解プロセス中、陰極が負電荷を生成するため、陽イオンが陰極に引き付けられます。陽イオンは、本質的に元素または複合体である可能性があります。陽イオン複合体には、正電荷を共有する一緒にグループ化されたいくつかの要素が含まれます。これは d ブロック要素に共通です。さらに、単一の元素は、酸化状態に応じて複数の陽イオンを持つことができます。すなわち、特異電荷、二重電荷、三重電荷など。いくつかの一般的な陽イオン 含む; Na、Ca、Feなど
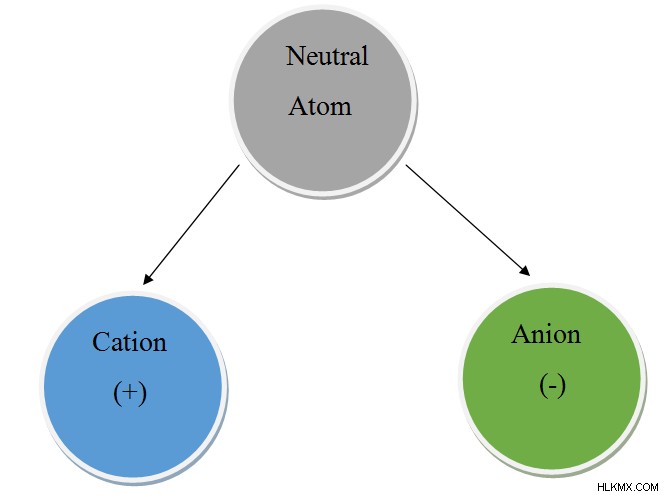
陰イオンとは
冒頭で述べたように、原子が電子を獲得すると陰イオンが形成されます。したがって、これらの電子の追加により、元素殻内の電子の数は、核内の陽子の数を超えます。陽子は正に帯電し、電子は負に帯電しているため、陰イオンは負の電荷を発生します。
通常、陰イオンは、希ガス配置を得ようとして、非金属元素によって形成されます。ギリシャ語で陰イオンという言葉は「上昇」を意味し、元素内の電子数の増加に関連している可能性があります。電気分解の過程で、陽極が正電荷を生成するため、陰イオンが陽極に引き付けられます。陰イオンは、本質的に元素または複合体である可能性があります。陰イオン複合体には、負電荷を共有する一緒にグループ化されたいくつかの要素が含まれます。これは d ブロック要素に共通です。また、単一の元素は、酸化状態に応じて複数の陰イオンを持つことができます。すなわち、特異電荷、二重電荷、三重電荷などです。いくつかの一般的な陽イオンには次のものがあります。 F、O、NO3 など
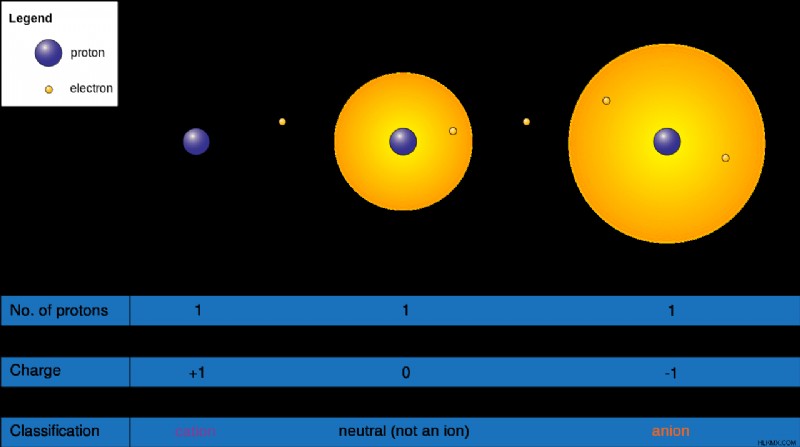
陽イオンと陰イオンの違い
定義
陽イオン 安定性を高めるために、その殻から 1 つまたは複数の電子を放出することによって生じる、正に帯電したイオンです
陰イオン 安定性を高めるために、1 つまたは複数の電子を殻に受け入れることによって生じる、負に帯電したイオンです。
チャージ
陽イオン
陰イオン
原子の形
陽イオン 通常、金属原子によって形成されます。
陰イオン 通常、非金属原子によって形成されます。
電気分解
陽イオン 陰極 (負電荷を生成する端) に引き付けられます。
陰イオン 陽極 (正電荷を生成する端) に引き寄せられます。
化合物の形成
陽イオン 陰イオンと静電相互作用を形成し、イオン化合物を形成します。
陰イオン 陽イオンと静電相互作用を形成し、イオン化合物を形成します。