1。何も起こりません(最も可能性が高い)
*分子は常に互いにぶつかります。 ほとんどの場合、彼らはお互いに跳ね返り、永続的な相互作用はありません。
*これは、分子が非極性である場合に特に当てはまります(強い正と負の領域がない)。
2。弱い相互作用
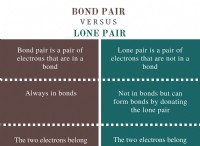
* van der Waals Force: これらは、電子分布の一時的な変動から生じる一時的な弱い魅力です。 それらは、液体の水を一緒に保持するなどのために重要です。
* 水素結合: これは、水素原子が酸素や窒素のような非常に感動性のある原子に結合されたときに発生するより強力な相互作用です。 それは、水の特性と生物学的分子において重要な役割を果たします。
* 双極子型相互作用: これらは極性分子間で発生し、1つの分子の正の端が別の分子の負の端に引き付けられます。
3。化学反応
*一部の分子は互いに反応し、新しい分子を形成することができます。 これには、分子が適切な「反応部位」と、活性化エネルギー障壁を克服するのに十分なエネルギーを持つことが必要です。
*反応の産物は、元の分子とは異なります。
4。凝集体の形成
*一部の分子は一緒に固執することができ、凝集体と呼ばれるより大きな構造を形成します。 これは、疎水性相互作用(非極性分子が一緒に群がり、水との接触を最小限に抑えるなど)など、さまざまな力によって駆動できます。
*例には、ミセル(水中の脂質球)とタンパク質複合体が含まれます。
5。 特定の例
* 水分子: 彼らは互いに水素結合を形成し、水に独自の特性を与えるネットワークを作成できます。
* DNA分子: 彼らは互いにベースペアをして、二重らせんを形成することができます。
* 化学反応中の反応物: 彼らは衝突して反応して新しい製品を形成することができます。
要約する:
* 2つの分子をまとめる結果は、それらの特定の特性と周囲の条件に依存します。
*何も起こらないことから、複雑な化学反応や新しい構造の形成にまで及ぶことができます。