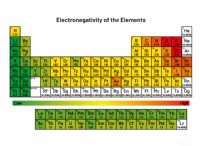
* アルカリ金属: これらの元素(リチウム、ナトリウム、カリウム、ルビジウム、セシウム、フランシウム)は、最も外側の殻に1つの電子しかありません。彼らは安定したオクテットを達成するためにこの電子を容易に失い、高度に反応します。 彼らは水、空気、その他多くの物質と激しく反応します。
* アルカリアース金属: まだ反応しますが、これらの金属(ベリリウム、マグネシウム、カルシウム、ストロンチウム、バリウム、ラジウム)は、最も外側の殻に2つの電子を持っています。安定したオクテットを達成するために2つの電子を失う必要があるため、アルカリ金属よりも反応性が低くなります。
* カーボンファミリー: このグループ(炭素、シリコン、ゲルマニウム、スズ、鉛)は、アルカリの金属やアルカリの地球金属よりも反応性が低くなっています。それらは多様な反応性パターンを示し、長い鎖と複雑な分子を形成する能力のために炭素は一意である。
* 不活性ガス: これらの要素(ヘリウム、ネオン、アルゴン、クリプトン、キセノン、ラドン)は最も反応性が低いです。 彼らは電子の完全な外側の殻を持っているため、それらは非常に安定しており、電子を獲得したり失ったりする可能性は低いです。
要約: 周期表でグループ(列)を下ると反応性が増加しますが、アルカリ金属は単一の原子価電子を容易に失う傾向があるため、最も反応的です。