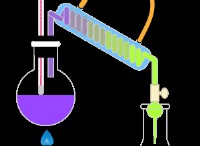
これがどのように機能しますか:
1。電解質: 分割する化合物は溶媒に溶解し、電解質溶液を作成します。この溶液にはイオン(荷電原子または分子)が含まれています。
2。電極: 2つの電極(通常はプラチナのような不活性金属製)が電解質に配置されています。 1つの電極は、直流(DC)電源(ANODE)の正端子に接続され、もう1つはネガティブ端子(カソード)に接続されています。
3。電流フロー: DC電源がオンになると、電流が電解質を流れます。
4。イオン移動: 電解質の正に帯電したイオン(陽イオン)は、負に帯電したカソードに引き付けられ、負に帯電したイオン(アニオン)は、正に帯電した陽極に引き付けられます。
5。酸化還元反応: 電極では、化学反応が起こります。
* 酸化: アノードでは、アニオンは電子(酸化)を失い、中性原子または分子を形成します。
* 削減: カソードでは、陽イオンは電子(還元)を獲得し、中性原子または分子を形成します。
例: 水の電気分解(H₂O)
* 電解質: 導電率を高めるために、少量の酸またはベースを含む水。
* 反応:
* アノード(酸化): 2H₂O→O₂ +4H⁺ +4E⁻
* カソード(還元): 4H⁺ +4E⁻→2H₂
* 全体的な反応: 2H₂O→2H₂ +o₂
本質的に、電流は化合物を保持する化学結合を克服するためのエネルギーを提供し、イオンが酸化還元反応を移動して受けることができ、最終的に化合物をその構成要素またはより単純な化合物に分割します。