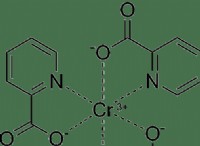
化学結合の主なタイプは次のとおりです。
1。イオン結合:
- 金属と非金属の間で発生します。
- 金属は電子を失い、正に帯電したイオン(陽イオン)を形成します。
- 非金属は電子を獲得して、負に帯電したイオン(アニオン)を形成します。
- 反対に帯電したイオンは互いに静電的に引き付け、強いイオン結合を形成します。
- 例:ナトリウム(Na)は1つの電子を失い、Na+になりますが、塩素(Cl)は1つの電子を獲得してCl-になります。それらは、静電引力のためにイオン化合物塩化ナトリウム(NaCl)を形成します。
2。共有結合:
- 2つの非金属間で発生します。
- 原子は電子を共有して、安定した電子構成を実現します。
- 共有電子は、原子を一緒に保持し、強い共有結合を作成します。
- 例:2つの水素原子(H)はそれぞれ1つの電子を共有して共有結合を形成し、分子H2を形成します。
3。金属結合:
- 金属原子間で発生します。
- 金属原子は、金属全体で自由に移動できる「電子の海」で価数電子を共有します。
- 電子のこの自由な動きは、導電率や閉鎖性などの金属の特徴を説明しています。
化学反応に影響する要因:
- 電気陰性度: 原子が電子を引き付ける傾向。要素間の電気陰性度の大きな違いはイオン結合を支持しますが、小さな違いは共有結合を支持します。
- 価電子: 原子の最も外側のシェルの電子の数は、形成できる結合の数を決定します。
- 反応条件: 温度、圧力、触媒の存在は、化学反応の速度と種類に影響を与える可能性があります。
化学反応の理解:
- 化学反応には、化学結合の破壊と形成が含まれます。
- エネルギーは発熱反応中に放出されますが、エネルギーは吸熱反応中に吸収されます。
- 化学式は、反応物と生成物を示す化学反応を表すために使用されます。
要約:
元素は、化学結合を介して電子を共有または伝達することにより、化合物を形成するように反応します。結合のタイプは、関与要素の電気陰性度と価電子に依存します。化学反応はさまざまな要因の影響を受け、独自の特性を持つ新しい物質の形成につながります。