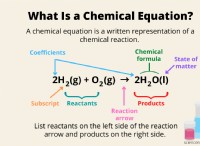
1。バランスの取れた化学式
エチレン(c₂h₄)と水(h₂o)の間の反応は、エタノール(c₂h₅oh)を生成します。
c₂h₄ +h₂o→c₂h₅oh
2。モル比
バランスの取れた方程式から、1モルのエチレンが1モルの水と反応することがわかります。これは、エチレンの水と水のモル比が1:1であることを意味します。
3。エチレンのモルを計算します
モル比は1:1であるため、0.0126モルの水と反応するには0.0126モルのエチレンが必要です。
4。モールをグラムに変換します
* エチレンのモル質量(c₂h₄): 2(12.01 g/mol) + 4(1.01 g/mol)=28.05 g/mol
* エチレンのグラム: (0.0126 mol) *(28.05 g/mol)= 0.353 g
したがって、0.0126モルの水と反応するには、0.353グラムのエチレンが必要です。