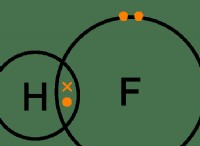
* 酸素の電気陰性度: 酸素は非常に電気陰性であり、炭素よりも強く電子を引き付けることを意味します。
* 不平等な共有: エーテルでは、酸素原子はC-O結合の共有電子をそれ自体に近づけ、酸素に部分的な負電荷(Δ-)を作成し、炭素原子に部分的な正電荷(Δ+)を作成します。電子のこの不平等な共有は、結合極性を作ります。
例: ジエチルエーテル(CH3CH2OCH2CH3)では、酸素原子は部分的な負電荷を持ち、結合した炭素原子には部分的な正電荷があります。
ただし、エーテルはそれほど極性ではないことに注意することが重要です 全体。酸素原子の両側にある2つのアルキル基(R)は、非極性であり、C-O結合の極性のバランスをとる傾向があります。これが、エーテルがアルコールと比較して比較的低い沸点を持っている理由です。