イオン結合 反対に帯電したイオン間の静電引力です。 ではありません 共有結合の基礎である電子の共有と同じ 。
これが故障です:
* イオン結合:
* 1つの原子は電子を失います(正に帯電したイオン - 陽イオンになります)。
*別の原子は電子を獲得します(負に帯電したイオンになります - 陰イオン)。
*反対の電荷が引き付けられ、強い静電結合が形成されます。
*例:NaCl(塩)、MGO(酸化マグネシウム)
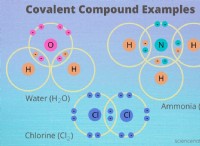
* 共有結合:
* 2つの原子が電子を共有して、安定した電子構成を実現します。
*彼らは、それぞれ1、2ペア、または3組の電子を共有し、それぞれ単一、二重、または三重の結合を形成できます。
*例:h₂o(水)、CO₂(二酸化炭素)
要するに、イオン結合には電子の伝達が含まれますが、共有結合には電子の共有が含まれます。