その理由は次のとおりです。
* ノーブルガスには、最も安定した電子構成があります。 彼らは電子の完全な外側の殻を持っているので、それらは非常に反応しません。これが、それらがしばしば「不活性ガス」と呼ばれる理由です。
* 他の要素は、貴重なガス構成を実現するよう努めています。 他の元素の原子は、電子を獲得、失い、または共有して、最も近い貴族の安定した電子構成を実現します。これは化学的結合の背後にある原動力です。
例:
* ナトリウム(Na) 外側のシェルに1つの電子があります。この電子を失うことにより、それは貴族であるNeon(NE)と同じ電子構成で正の帯電イオン(Na+)になります。
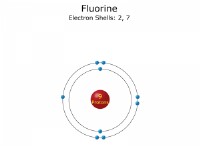
* 塩素(cl) 外側のシェルに7つの電子があります。 1つの電子を獲得することにより、nobleガスであるArgon(AR)と同じ電子構成を備えた負に帯電したイオン(CL-)になります。
そのため、安定した構成のために、貴族は不活性ですが、他の要素は同じレベルの安定性を達成しようとするため、反応します。