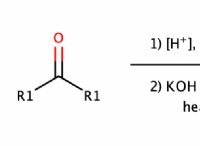
* 二酸化炭素(CO2): その液相では、CO2は非電解質です 。溶液中の荷電種(イオン)に容易にイオン化することはありません。これは、CO2が強い共有結合を持つ分子化合物であるためです。
* 塩化ナトリウム(NaCl): 水に溶解すると、塩化ナトリウムは強い電解質です 。 それは完全にイオンに分離します:
*na⁺(ナトリウムイオン)
*cl⁻(塩化物イオン)
* 蒸留水(H2O): 純粋な蒸留水は、非常に弱い電解質です 。 それはわずかな自己イオン化を受け、わずかな量のH⁺(水素イオン)とOH⁻(水酸化物イオン)を生成します。
* 過酸化水素(H2O2): その液相では、過酸化水素は弱い電解質です 。それは部分的にH⁺(水素イオン)およびHO2⁻(ヒドロペルオキシドイオン)にイオン化します。
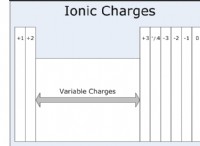
キーテイクアウト:
* 電解質 溶媒(水など)に溶解すると電気を伝達する物質です。この導電率は、遊離イオンの存在から生じます。
* 強い電解質 溶液中に完全にイオン化し、高濃度のイオンを生成します。
* 弱い電解質 溶液中に部分的にイオン化し、低濃度のイオンを生成します。
* 非電解質 溶液中にまったくイオン化しないでください。