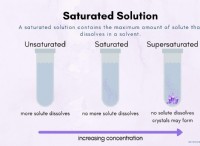
* 質量の保存: 化学方程式のバランスをとることの基本原則は、質量の保存です。これは、各要素の原子の総数が方程式の両側で同じでなければならないことを意味します。
* 一意の比率: バランスの取れた方程式は、反応と化学反応で形成される反応物と生成物の特定の比を表します。この比率は一意であり、質量の保存を維持しながら変更することはできません。
例:
水素と酸素の間の反応を考えて水を形成します。
*不均衡:h₂ +o₂→h₂o
*バランス:2h₂ +o₂→2h₂o
このバランスの取れた方程式を4H₂ +2O₂→4H₂Oとして書くこともできますが、それでも水素、酸素、水と同じ比率(2:1:2)を表しています。
キーポイント:
* 最も単純な全自由比: バランスの式は、通常、係数の最も単純な全自由比を使用して表されます。
* 同等の表現: バランスの取れた方程式を表現する複数の方法が存在しますが、それらはすべて最終的には反応物と生成物の同じ比を表します。
したがって、バランスのとれた方程式を書くにはさまざまな方法があるかもしれませんが、正しい化学量論比を表す最終バランスの式は常に同じです 。