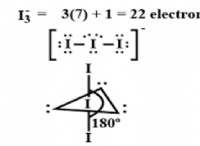
1。電子構成:
*アルカリ金属には、 1つの価電子のみがあります 最も外側のシェルに。この単一の電子は、原子にゆるく結合されています。
*この構成により、彼らはこの電子を失い、Nobleガスと同様に安定したOctet構成を実現することに熱心になります。
2。低イオン化エネルギー:
*イオン化エネルギーは、原子から電子を除去するのに必要なエネルギーです。アルカリ金属には、非常に低いイオン化エネルギーがあります 。これは、単一の原子価電子を除去するのに非常に少ないエネルギーが必要なことを意味します。
3。大きな原子半径:
*アルカリ金属には大きな原子半径があります 。それらの最も外側の電子は核から遠く離れており、魅力が少なくなります。これにより、電子の除去が容易になります。
4。弱い金属結合:
*アルカリ金属の金属結合は弱いです ゆるく保持された価電子電子のため。これにより、イオンを簡単に形成し、化学反応に参加できます。
反応性の結果:
* 空気との反応: アルカリ金属は、空気中の酸素と容易に反応して酸化物を形成します。この反応はしばしば発熱性であり、暴力的である可能性があります。
* 水との反応: アルカリ金属は水と激しく反応し、水素ガスと対応する水酸化物の溶液を生成します。この反応は非常に発熱性であり、爆発的である可能性があります。
* ハロゲンとの反応: アルカリ金属はハロゲンと反応してイオンハロゲン化物を形成します。これらの反応も発熱性です。
要約: 電子構成、低イオン化エネルギー、大きな原子半径、および弱い金属結合の組み合わせにより、アルカリ金属は非常に反応します。彼らは、安定性を達成するために原子価の電子を容易に失い、さまざまな物質との激しい反応につながります。