理由:
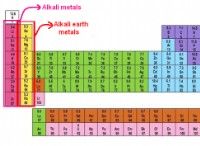
* 電気陰性度: アルカリ金属は電気陰性度が低いため、電子を容易に失い、陽性イオンを形成します。これにより、酸素と非常に反応性が高くなります。これは非常に感動的であり、電子を容易に獲得します。
* イオン化エネルギー: アルカリ金属のイオン化エネルギーは低いため、最も外側のシェルから電子を除去するために必要なエネルギーが少なくなります。これにより、金属酸化物の形成が促進されます。
* 金属文字: アルカリの金属は非常に金属製です。つまり、陽イオンを容易に形成し、電子を寄付する傾向が強いことを意味します。
例:
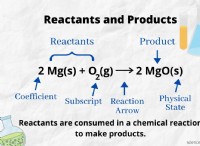
* ナトリウム(Na) 酸素と激しく反応して、酸化ナトリウム(Na₂O)を形成します。
* カリウム(k) 酸素とさらに激しく反応して、酸化カリウム(K₂O)を形成します。
対照的に、コインメタルは電気陰性度が高く、イオン化エネルギーが高く、金属が少ない。 これにより、酸素との反応性が低下します。
例:
* 銅(Cu) 水分の存在下で酸素とゆっくりと反応して、酸化銅(CUO)を形成します。
* シルバー(Ag) 室温での酸素と比較的反応しません。
* 金(au) 酸化に対して非常に耐性があります。
結論:
電気陰性度が低く、イオン化エネルギーが低く、金属特性が高いため、グループ1要素(アルカリ金属)は、グループ11要素(硬貨金属)よりも酸素とはるかに反応します。