シュウ酸(h₂c₂o₄)で過マンガン酸カリウム(Kmno₄)の滴定
酸化還元反応:
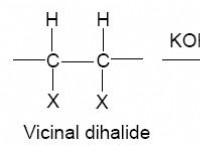
* 酸化: H₂C₂O₄(シュウ酸)→2Co₂ +2H⁺ +2e⁻
* 削減: mno₄⁻(パルマンガン酸イオン) +8h⁺ +5e⁻→mn²⁺(マンガンイオン) +4h₂o
なぜインジケータが必要なのか:
* 過マンガン酸の自己指示: 過マンガン酸カリウム(Kmno₄)自体は、弱い指標として機能します。 溶液中の深い紫色は、ほぼ無色のmn²⁺イオンに縮小すると消えます。ただし、この色の変化は、正確な滴定のために十分にシャープではありません。
* クリアエンドポイントの必要性: 滴定のエンドポイント(反応が完了する場合)は、色の変化がある場合、より明確に見えます 発生します。
使用されたインジケーター:
* 通常、外部インジケータは使用されません。 過マンガン酸溶液は、独自の指標として機能します。過マンガン酸溶液の最後のドロップの後に持続するかすかなピンク色は、エンドポイントに信号を追加します。
説明:
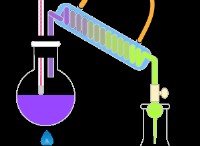
1。初期セットアップ: 既知の容量のシュウ酸溶液をフラスコに入れます。
2。滴定: 過マンガン酸カリウムの標準溶液を、シュウ酸溶液に滴下します。 紫色の過マンガン酸溶液は、無色のシュウ酸と反応します。
3。エンドポイント: パルマンガン酸イオンのかすかなピンク色がフラスコで持続すると、反応は完全です。これは、すべてのシュウ酸が酸化されていることを示しています。
キーポイント:
* 酸化還元反応: この反応には、シュウ酸(酸化)から過マンガン酸(減少)への電子の伝達が含まれます。
* インジケーター: 過マンガン酸自体はインジケータとして機能します。
* エンドポイント: エンドポイントは、かすかなピンク色の永続性によってマークされています。
他の例を調査したい場合は、この特定の反応の化学を深く掘り下げたい場合はお知らせください。