その理由は次のとおりです。
* イオン化合物: 塩はイオン化合物です。つまり、積極的に帯電したイオン(陽イオン)と、静電力によって結合された負に帯電したイオン(アニオン)で構成されています。
* 極水分子: 水分子は極性であり、水素側にわずかに正電荷で、酸素側にわずかに負の電荷があります。
* アトラクションと解離: 水分子の正と負の端は、塩結晶内の反対に帯電したイオンに引き付けられます。この魅力は、結晶内でイオンを一緒に保持する力を克服し、塩を個々のイオンに分離(分解)します。
例:
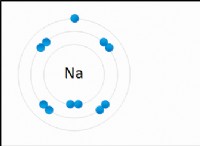
テーブル塩(NaCl)が水に溶解すると、ナトリウムイオン(Na+)および塩化物イオン(CL-)に分解します。
NaCl(s)→Na +(aq) + cl-(aq)
「(aq)」は、イオンが水に溶解し、水溶液を形成することを示しています。