1。溶解度:
* "like like dislols like": 極性分子は、他の極性分子(たとえば、砂糖の溶解)を溶解するのに適しています。 これは、両方の分子の部分的な正電荷と負の電荷が、それらをまとめる強力な静電相互作用(水素結合、双極子双極子相互作用)を形成できるためです。
* 不混和性: 極性分子は一般に、非極性分子(油や水など)とうまく混ざりません。これは、非極性分子に電荷が不足しているため、極性分子との強い相互作用の形成が妨げられるためです。
2。反応性:
* 極性は反応速度を向上させます: 極性分子の部分的な電荷は、化学反応における荷電中間体と遷移状態を安定させるのに役立ち、これらの反応をより速く進めることができます。
* 求核反応: 極性分子は、しばしば求核症(電子が豊富な種)または電気飼料(電子欠損種)として作用し、広範囲の化学反応につながります。
3。物理的特性:
* 沸点と融点: 極性分子は一般に、それらが形成する強い分子間力により、非極性分子と比較して沸点と融点が高くなります。
* 表面張力: 水の強い極性は表面の張力が高く、その表面上の小さな物体(昆虫のような)を支えることができます。
例:
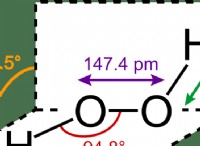
* 水: 水は非常に極性分子であり、多くの物質にとって優れた溶媒となっています。
* エタノール: エタノールのヒドロキシル基はそれを極性にし、水に溶解して溶媒自体として作用することができます。
* タンパク質とDNA: タンパク質の極アミノ酸とDNAの極リン酸基は、その水溶解度と全体的な構造に寄与します。
* 洗剤: 洗剤は、極性と非極性部品の両方を持つように設計されています。極地は水と相互作用し、非極性部分はグリースとオイルと相互作用し、これらの物質を溶解できるようにします。
要約: 極性は化学の世界で強力な力です。物質がどのように相互作用し、溶解し、反応し、振る舞うかを決定し、私たちの調理方法から生命そのものの基礎まですべてに影響を与えます。