その理由は次のとおりです。
* 酸 水に溶解すると水素イオン(H+)を放出する物質です。
* 水素イオン 水分子の部分的に負の酸素原子に引き付けられます。
*このアトラクションは水素結合を形成します 、これは、水分子を一緒に保持するのに役立つ強力な分子間力です。
水素を水に結合するイオンを形成する酸の例:
* 塩酸(HCl): HClが水に溶解すると、H+イオンと塩化物イオン(CL-)を放出します。 H+イオンは、水分子と水素結合を形成します。
* 硫酸(H2SO4): 硫酸は分子あたり2つのH+イオンを放出し、水中の水素結合ネットワークをさらに強化します。
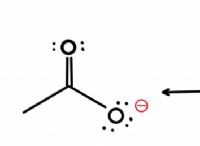
* 酢酸(CH3COOH): 酢には、水の水素結合構造に寄与する酢酸が含まれています。
注: 酸はH+イオンを放出しますが、H+イオンを放出するすべての化合物が酸であるわけではありません。たとえば、一部の塩は、水に溶解するとH+イオンを放出することもできますが、酸とは見なされません。