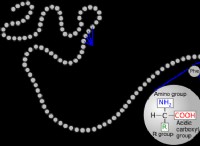
* 陽子: 原子の核に見られる正に帯電した粒子。プロトンの数は、原子の要素を定義します(たとえば、すべての炭素原子には6つのプロトンがあります)。
* 中性子: 中性帯電した粒子も核に見られます。中性子は原子の質量に寄与しますが、その電荷ではありません。元素の異なる同位体には、同じ数のプロトンがありますが、さまざまな数の中性子があります。
* 電子: シェルまたはエネルギーレベルで核を周回する負に帯電した粒子。電子は、陽子や中性子よりもはるかに小さくて軽いです。中性原子の電子の数は、プロトンの数に等しくなります。
追加情報:
*陽子と中性子は、集合的に核子として知られています 、彼らが原子の核を構成するとき。
*原子はほとんど空のスペースです。核は非常に密度が高く、ほとんどすべての原子の質量が含まれていますが、原子体積のごく一部しか占めていません。
*電子は常に動いており、その正確な位置を正確に決定することはできません。代わりに、軌道として知られる特定の空間領域で電子を見つける可能性について話します 。
これら3つを超えた他の亜原子粒子もありますが、それらは原子の構造の基本ではなく、通常、高エネルギー物理学でのみ遭遇します。