* 電子構成: 炭素には6つの電子があり、最初のシェルに2つ、外側(価)シェルに4つの電子があります。
* オクテットルール: 原子は、電子を獲得、失い、または共有する傾向があり、外側のシェルに8つの電子を備えた安定した構成を実現します(オクテットルール)。
* カーボンの目標: 炭素は、安定したオクテットに到達するために、さらに4つの電子を獲得する必要があります。
* 結合: 炭素は、4つの共有結合を形成することによりこの安定性を達成し、他の4つの原子のそれぞれと1つの電子を共有します。
ここに炭素が非常に特別な理由があります:
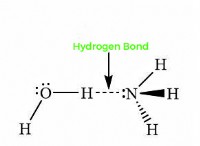
* 汎用性: 炭素は、水素、酸素、窒素、その他の炭素を含む他のさまざまな要素と結合できます。これにより、幅広い多様な有機分子が可能になります。
* 鎖の形成: 炭素は、それ自体で長いチェーンとリングを形成し、複雑な構造につながる可能性があります。この能力は、タンパク質、炭水化物、核酸などの大きな生物学的分子の形成の基本です。
本質的に、4つの結合を形成するカーボンの能力は、安定した電子構成を達成したいという欲求によって推進されており、非常に多様で複雑なオーガニック化学の世界につながります。