主な違い – レンチウイルスとレトロウイルス
レンチウイルスとレトロウイルスは、ライフサイクルを完了するために生きた細胞に感染する 2 種類のウイルス です。レンチウイルスはレトロウイルスの亜型です。 主な違い レンチウイルスとレトロウイルスの違いは、レンチウイルスは活発に分裂している細胞と分裂していない細胞の両方に感染できるのに対し、レトロウイルスは有糸分裂が活発な細胞タイプにしか感染できないことです。 .したがって、レンチ ウイルスはレトロ ウイルスよりも広い範囲の細胞段階に感染できます。レンチウイルスとレトロウイルスの両方が、外来DNA分子を別の細胞に運ぶ媒体として使用できます。ウイルスによって媒介される DNA 転送のメカニズムは、形質導入として知られています。レンチウイルスとレトロウイルスの両方が、疾患の発症に関与する欠陥のある遺伝子を修正するために使用されます。
対象となる主な分野
1.レンチウイルスとは
– 定義、プロパティ、タイプ
2.レトロウイルスとは
– 定義、プロパティ、タイプ
3.レンチウイルスとレトロウイルスの類似点は何ですか
– 共通機能の概要
4.レンチウイルスとレトロウイルスの違いは何ですか
– 主な相違点の比較
重要な用語:HIV、レンチウイルス、組換え DNA テクノロジー、レトロウイルス
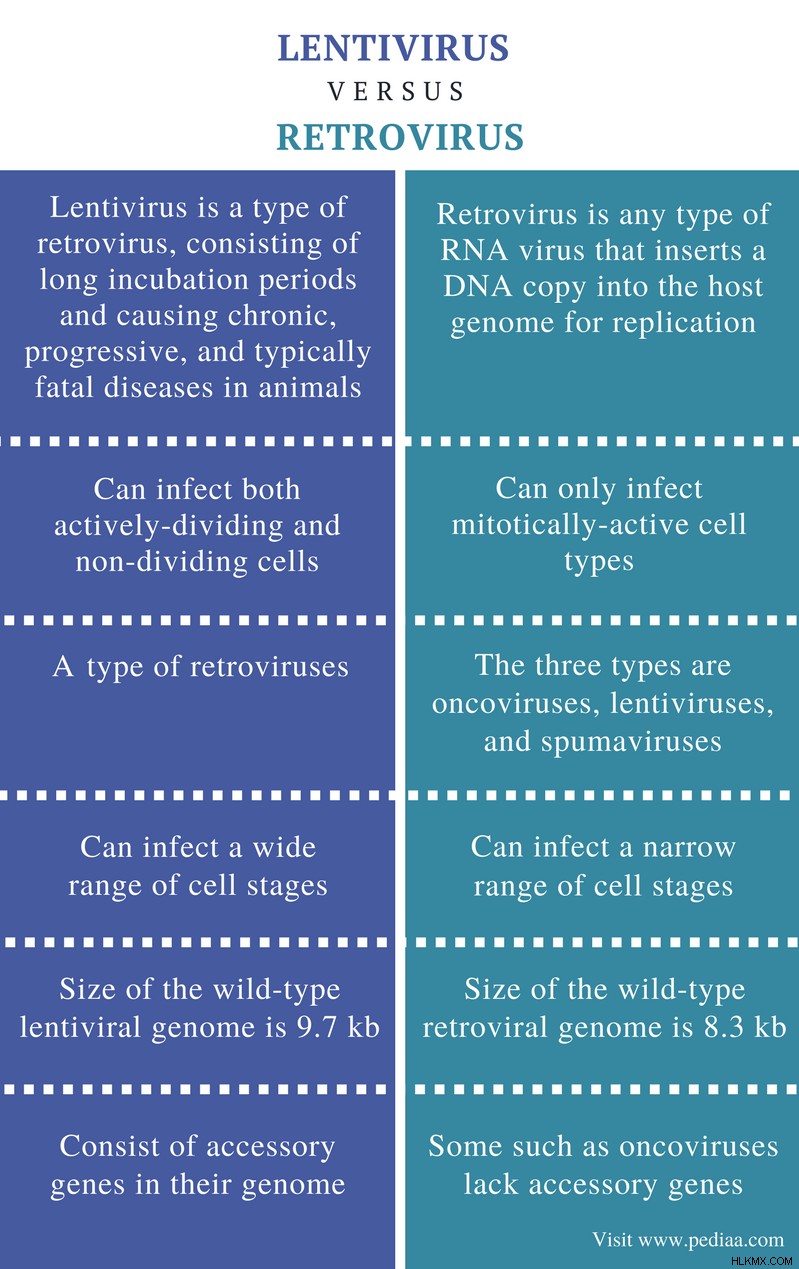
レンチウイルスとは
レンチウイルスはレトロウイルスの一種で、潜伏期間が長く、動物に慢性、進行性、および通常は致命的な病気を引き起こします。レンチウイルスは、感染する脊椎動物宿主の種類に基づいて 5 つの血清型に細分化できます。ウシ、ウマ、ネコ、ヒツジ/ヤギ、および霊長類。ヒト免疫不全ウイルス (HIV) 2 型、サル (SIV)、およびネコ (FLV) は、レンチウイルスの例です。レンチウイルスは、大きな DNA セグメントを細胞株 (分裂)、初代細胞 (分裂および非分裂)、神経細胞、幹細胞、および造血細胞に導入するために使用されます。ほとんどのレンチウイルスベクターは HIV に基づいています。 HIV の構造を図 1に示します。

図 1:HIV
HIV ゲノムのサイズは 9.7 kb です。ゲノムに存在する 3 つの主要な構造遺伝子は gag です。 (グループ特異抗原)、pol (ポリメラーゼ)、および env (封筒)。他の調節遺伝子は tat です (HIV トランス活性化因子) および rev (ビリオンタンパク質の発現調節因子)。さらに、4 種類のアクセサリー遺伝子も HIV ゲノムに存在します:vif (ウイルス感染性)、vpr (ウイルス プロテイン R)、vpu (ウイルスタンパク質 U)、および nef (マイナス要因)。レンチウイルスの複製、統合、およびパッケージングは、レンチウイルスゲノムのシス作用エレメントによって媒介されます。
レトロウイルスとは
レトロウイルスは、複製のために宿主ゲノムに DNA コピーを挿入する RNA ウイルスの一種です。レトロウイルスは、RNA ゲノムを逆転写して、宿主ゲノムに組み込むことができる cDNA コピーにする能力を特徴としています。それらは、ゲノム内のポジティブセンス ssRNA 分子の 2 つのコピーで構成されます。レトロ ウイルスは、ゲノムに存在するさまざまなタイプのアクセサリーおよび調節遺伝子に基づいて、3 つのサブファミリーに分類できます。それらは、オンコウイルス、レンチウイルス、およびスプマウイルスです。オンコウイルスは、形態に基づいて 3 つのカテゴリに分類されます。 B型、C型、D型。レトロウイルスのさまざまなサブファミリーと例を表1に示します。
レトロウイルスのサブファミリーと例
| レトロウイルス サブファミリー | 例 |
オンコウイルス B 型 | マウス乳腺腫瘍ウイルス (MMTV) |
| オンコウイルスC型 | ヒト T 細胞白血病ウイルス (HTLV)、鳥類白血病および肉腫ウイルス (ALSV)、サーモン リンパ腫ウイルス |
| オンコウイルス D 型 | メイソンファイザーサルウイルス (MPMV) |
| レンチウイルス | ヒト免疫不全ウイルス (HIV)、ヒツジマエディビスナウイルス (MVV)、馬伝染性貧血ウイルス (EIAV) |
| スプマウイルス | シミアン フォーミー ウイルス (SFV) |
レトロウイルスは、RNA ゲノムを逆転写する逆転写酵素で構成されています。カプシド (CA)、ヌクレオカプシド (NC)、インテグラーゼ (IN)、プロテアーゼ (PR) などの構造タンパク質と酵素タンパク質は、レトロウイルス コンパートメント内にあります。
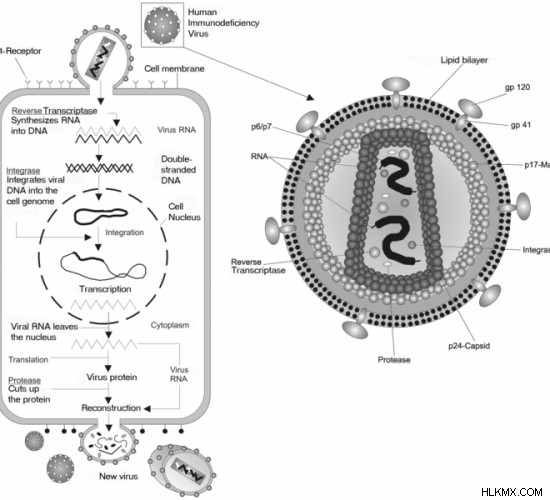
図 2:HIV 感染メカニズム
レトロウイルスの内核は、マトリックス (MA) タンパク質からなる外側のタンパク質層に囲まれています。レトロウイルスのエンベロープは、宿主細胞膜に由来します。レトロウイルスは、分裂細胞株、初代細胞、幹細胞、造血細胞に感染します。
レンチウイルスとレトロウイルスの類似点
- レンチウイルスとレトロウイルスは、生きた細胞に感染する 2 種類のウイルスです。
- レンチウイルスとレトロウイルスのキャプシドは正二十面体の形をしており、どちらもエンベロープウイルスです.
- レンチウイルスとレトロウイルスはどちらも、プラスセンス ssRNA ゲノムの 2 つのコピーで構成されています。
- レンチウイルスとレトロウイルスはどちらも逆転写酵素 (RT) で構成されています。
- レンチウイルスとレトロウイルスはどちらも、RNA ゲノムを逆転写して cDNA コピーにすることができます。
- レンチウイルスとレトロウイルスの両方のゲノムは、ポリメラーゼのためにコード化されています.
- レンチウイルスとレトロウイルスはどちらも、外来 DNA 分子を別の細胞に運ぶ媒体として使用できます。
- レンチウイルスとレトロウイルスはどちらも組換え DNA 技術で使用され、比較的大きな外来 DNA セグメントを動物細胞に導入します。
- 遺伝子治療では、レンチウイルスとレトロウイルスの両方が使用され、病気の発症の原因となる欠陥遺伝子を修正します。
- レンチウイルスとレトロウイルスは、gag の異なるアイソフォームを使用します 、柱 、および env パッケージングの遺伝子
- レンチウイルスとレトロウイルスはどちらも分裂細胞、幹細胞、造血細胞に感染します。
- レンチウイルスとレトロウイルスはどちらも幅広い宿主範囲を持っています.
- レンチウイルスとレトロウイルスの両方のインサートのサイズは約 8.0 kb です。
- レンチウイルスとレトロウイルスの両方の DNA がゲノムに組み込まれています。
- レンチウイルスとレトロウイルスの両方を最大 10 コピーまで統合できます。
- レンチウイルスとレトロウイルスの両方で、タンパク質の発現レベルはそれほど高くありません.
- レンチウイルスとレトロウイルスの推奨バイオセーフティレベルはBSL-2です。
レンチウイルスとレトロウイルスの違い
定義
レンチウイルス: レンチウイルスはレトロウイルスの一種で、長い潜伏期間を持ち、動物に慢性、進行性、そして通常は致命的な病気を引き起こします.
レトロウイルス: レトロウイルスは、複製のために宿主ゲノムに DNA コピーを挿入する RNA ウイルスの一種です。
感染細胞の種類
レンチウイルス: レンチウイルスは、活発に分裂している細胞と分裂していない細胞の両方に感染できます。
レトロウイルス: レトロウイルスは有糸分裂活性のある細胞型にのみ感染できます。
タイプ
レンチウイルス: レンチウイルスはレトロウイルスの一種です。
レトロウイルス: レトロウイルスには、オンコウイルス、レンチウイルス、スプマウイルスの 3 種類があります。
範囲
レンチウイルス: レンチウイルスは、幅広い細胞段階に感染する可能性があります。
レトロウイルス: レトロウイルスは、狭い範囲の細胞段階に感染する可能性があります.
ゲノムのサイズ
レンチウイルス: 野生型レンチウイルスゲノムのサイズは 9.7 kb です。
レトロウイルス: 野生型レトロウイルスゲノムのサイズは 8.3 kb です。
アクセサリー遺伝子
レンチウイルス: レンチウイルスは、ゲノム内のアクセサリー遺伝子で構成されています。
レトロウイルス: オンコウイルスなどの一部のレトロウイルスは、アクセサリー遺伝子を欠いています。
結論
レンチウイルスとレトロウイルスは、生きた細胞に感染する 2 種類のウイルスです。レンチウイルスはレトロウイルスの一種です。レンチウイルスとレトロウイルスはどちらも組換え DNA 技術で使用され、比較的大きな外来 DNA セグメントを動物細胞に導入します。レンチウイルスは分裂細胞と非分裂細胞の両方に感染できますが、レトロウイルスは分裂細胞にしか感染できません。これがレンチウイルスとレトロウイルスの主な違いです。
参照:
1. O'Keefe、Eric P.「核酸送達:レンチウイルスおよびレトロウイルスベクター」。 材料と方法 、2015 年 6 月 15 日、こちらから入手可能。
画像提供:
1. 「HI-Virion-en」米国国立衛生研究所 (en:User:Carl Henderson により再描画) – 米国国立衛生研究所 (en:User:Carl Henderson により再描画) (パブリック ドメイン)、Commons Wikimedia 経由
2. 「Hiv グロス」Raul654 による翻訳 – GFDL 画像からの原画像:Hiv グロス german.png (CC BY-SA 3.0) via Commons Wikimedia







