希ガスは、周期表の 18 族の元素です。これらの元素の原子は価電子殻を満たしているため、室温と圧力で比較的不活性、無色、無臭の単原子ガスになります。
なぜ希ガスは希ガスと呼ばれるのですか?
「希ガス」という用語は、ドイツ語の Edelgas の翻訳に由来します。 、希ガスを意味します。ドイツの化学者ヒューゴ・エルトマンは 1898 年にこの言葉を作り出しました。貴族が庶民と付き合うのは威厳がないと考えるように、希ガスは他の元素と反応しない傾向があります。
希ガスの他の名前には、希ガス、不活性ガス、およびエアロゲンが含まれます。周期表を参照すると、希ガスは IUPAC グループ 18 (古い方法ではグループ 0)、CAS グループ VIIIA、ヘリウム グループ、またはネオン グループです。
希ガスのリスト
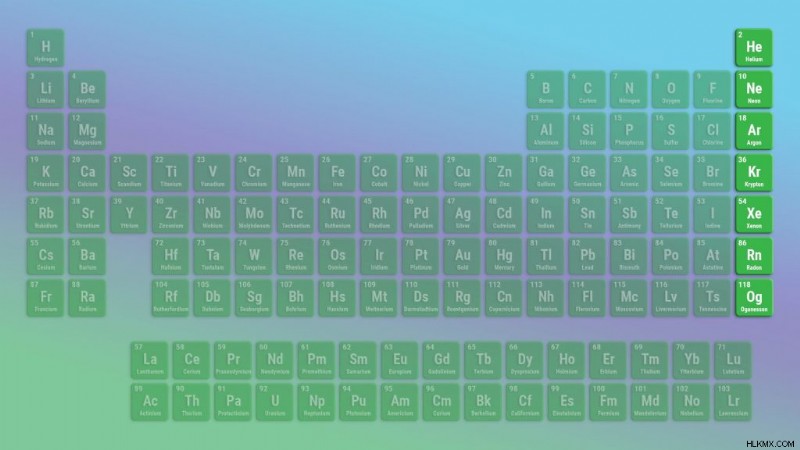
要素 118、オガネソンを含めるかどうかに応じて、6 つまたは 7 つの希ガス要素があります。
- ヘリウム (He)
- ネオン (Ne)
- アルゴン (Ar)
- クリプトン (Kr)
- キセノン (Xe)
- ラドン (Rn)
- オガネソン (Og)
最初の 6 つの要素は自然に発生します。ラドンとオガネソンは放射性元素です。 Oganesson は、グループに完全には適合しない人工 (合成) 要素です。満たされた原子価殻 (7p) を持っている可能性がありますが、室温では金属固体であると予測されています。
希ガスの性質
希ガス族の元素は、共通の化学的および物理的特性を共有しています:
- 標準条件下でほぼ理想的なガスとして振る舞う
- 室温での単原子ガス
- あまり反応しない
- 完全な外側の電子または原子価殻 (酸化数 =0)
- 高いイオン化エネルギー
- 非常に低い電気陰性度
- 低融点
- 低沸点
- 通常の状態では無色、無臭、または無味 (ただし、有色の液体や固体を形成する可能性があります)
- 不燃性
- 低圧で電気を通し、蛍光を発する
よくある誤解
希ガスに関する最も一般的な誤解は、希ガスは化学結合や化合物を形成できないというものです。それらの原子は通常、原子価殻で満たされていますが、1 つまたは複数の電子を除去したり、(あまり一般的ではありませんが) 電子を追加したりすることができます。特定の条件下では、希ガスは、二原子ガス、クラスレート、フッ化物、塩化物、金属錯体、およびその他の化合物を形成する可能性があります。通常、化合物は非常に高い圧力下で形成されます。希ガス化合物の例としては、フッ化水素化アルゴン (HArF) および六フッ化キセノン (XeF6 ).
別の誤解は、希ガスはまれであるということです。希土類と同様に、希ガスは特に珍しいものではありません。アルゴンは、大気中で 3 番目または 4 番目に豊富なガスです (水蒸気の量によって異なります)。それは、大気質量の 1.3% またはその体積の 0.94% を占めます。ネオン、クリプトン、ヘリウム、キセノンは空気中の微量元素です。ガスは、地球の奥深くでより豊富に存在する可能性があります。ヘリウムは天然ガスに含まれていますが、キセノンは一部の鉱泉からの蒸気に含まれており、地球のコアで鉄やニッケルと結合している可能性があります。
希ガスの使用
希ガスにはいくつかの重要な用途があります。それらは、試料を保護し、化学反応を最小限に抑えるための不活性雰囲気として使用されます。融点と沸点が低いため、冷媒として有用です。希ガスは、高輝度ランプ、ネオンライト、車のヘッドランプ、エキシマ レーザーなどの照明用途で重要です。ヘリウムは、気球、深海潜水用の呼吸ガス混合物、および超伝導マグネットの冷却に使用されます。ガス、特にキセノンは、イオン ドライブで使用されます。現在、オガネソンには実用的な用途はありませんが、いつか科学者がさらに重い元素を作るのに役立つかもしれません.
希ガス源
ネオン、アルゴン、クリプトン、キセノンは、液化空気の分別蒸留によって生成されます。ヘリウムの主な供給源は、天然ガスの極低温分離です。ラドンは、ラジウム、トリウム、ウラン、およびその他の重放射性元素の放射性崩壊から発生します。オガネソンは、加速された粒子をターゲットに当てることによって合成された人工の要素です。将来、希ガスは他の惑星から供給されるかもしれません。たとえば、ヘリウムとキセノンは、木星やその他のガス惑星では地球よりもはるかに豊富です。
参考文献
- Greenwood, N.N.;アーンショー、A. (1997)。 元素の化学 (第 2 版)。オックスフォード:バターワース・ハイネマン。 ISBN 0-7506-3365-4.
- Lehmann, J (2002). 「クリプトンの化学」。 配位化学のレビュー . 233–234:1–39。 doi:10.1016/S0010-8545(02)00202-3
- 小島 稔; Podosek、フランク A. (2002)。 希ガス地球化学 .ケンブリッジ大学出版局。 ISBN 0-521-80366-7.
- Partington, J. R. (1957). 「ラドンの発見」。 自然 . 179 (4566):912. doi:10.1038/179912a0
- ルヌーフ、エドワード (1901)。 「希ガス」。 科学 . 13 (320):268–270.