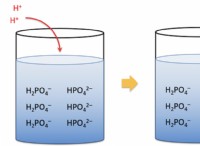
化合物が強力な電解質であるかどうかを調べると、化合物と分子を構成するさまざまな種類の化学結合をさらに区別するのに役立ちます。強力な電解質は、溶液中の陽イオンと陰イオンに完全に解離する化合物です。溶液中で電気をよく伝導します。化合物は、強電解質または弱電解質のいずれかになります。それぞれ異なる特性を持っているため、それらを区別できることが重要です。
<オール>化合物がイオン性か共有結合かを判断します。イオン性化合物は、通常、金属と非金属で構成されています。水素を除く金属は周期表の左側にあり、非金属は右側にあります。イオン性化合物の例は、KCl、または塩化カリウムです。共有結合化合物は、通常、非金属で構成されています。例は、C2H6、またはエタンです。化合物が共有結合である場合、それはおそらく強力な電解質ではありません。イオン性化合物は強い電解質である可能性が高くなります.
化合物が強酸であるかどうかを分析します。強酸は強電解質でもあります。 HCl、HBr、HI などの 17 族の元素から形成される化合物は強酸です。他の強酸には、H2SO4、HNO3、HClO3、HClO4 などがあります。
化合物が強塩基かどうかを調べます。強塩基は強電解質でもあります。水酸化物イオン OH- で形成される化合物は、通常、強塩基です。例としては、LiOH、NaOH、KOH、Ca(OH)2、Ba(OH)2 などがあります。
化合物が 17 族の元素と 1 族または 2 族の元素から形成されているかどうかを判断します。このような化合物は通常、強い電解質でもあるイオン塩です。例としては、NaCl や KCl などがあります。
亜鉛と銅で形成される強力な電解質を覚えておいてください。強力な電解質である 2 つの化合物は、イオン化合物 ZnSO4 と CuSO4 です。化合物がこれらのいずれかである場合、それは間違いなく強力な電解質です.
必要なもの
- 周期表
- コンピューター
- 化学の本