主な違い - シグマとパイボンド
シグマ結合とパイ結合は、共有結合と 3 つまたは 2 つの原子を持つ分子のいくつかの特徴を表すために使用されます。これらの結合は、不完全な s の重なりによって形成されます および p 結合に関与する 2 つの原子の軌道。したがって、このモデルはしばしば重複モデルと呼ばれます。このモデルは、主に小さな原子の結合形成を説明するために適用され、大きな分子の結合を説明するには適用できません。シグマ結合とパイ結合の主な違いは、それらの形成です。 2 つの軌道の軸方向の重なりがシグマ結合を形成 2 つの軌道の横方向の重なりがパイ結合を形成 .
この記事では、
1.シグマボンドとは
– 定義、特性、プロパティ
2. Piボンドとは
– 定義、特性、プロパティ
3.シグマとパイボンドの違いは何ですか
シグマ ボンドとは
2 つの原子の原子軌道が同軸または線形に重なり合うと、シグマ結合が形成されます。単結合、二重結合、三重結合に含まれる主要な結合です。ただし、2 つの原子間に存在できるシグマ結合は 1 つだけです。シグマ結合は原子軌道の重なりが最大であるため、シグマ結合はパイ結合よりも強力です。結合軸に沿って位置する単一の電子雲が含まれています。シグマ結合は、共有結合の形成中に形成される最初の結合です。パイ結合とは異なり、混成軌道と非混成軌道の両方がシグマ結合を形成します。
Pi ボンドとは
Pi 結合は、原子軌道の横方向または横方向または平行な重なりによって形成されます。これらの結合は、重なり合う範囲が最小限であるため、シグマ結合よりも弱いです。また、シグマ結合が形成された後にパイ結合が形成されます。したがって、これらの結合はシグマ結合とともに常に存在します。パイ結合は、ハイブリダイズしていない p-p 原子軌道の重なりによって形成されます。シグマ結合とは異なり、パイ結合は分子の形状に影響を与えません。単結合はシグマ結合です。しかし、二重結合と三重結合には、シグマ結合とともに、それぞれ 1 つと 2 つのパイ結合があります。
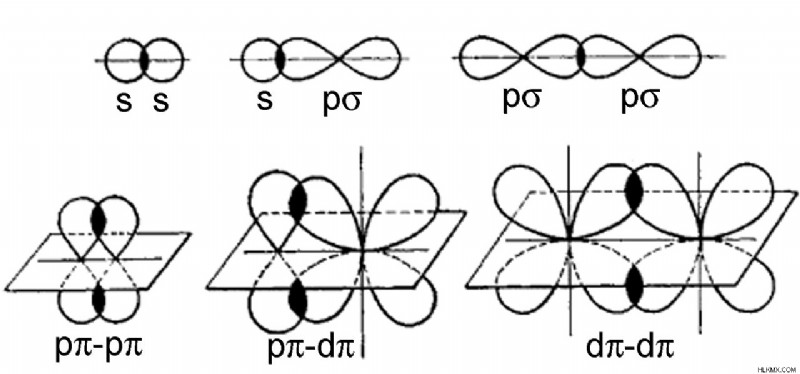
図 01:シグマ結合とパイ結合
シグマとパイボンドの違い
絆の形成
シグマ ボンド: シグマ結合は、原子の半分満たされた原子軌道の軸方向の重なりによって形成されます.
パイボンド: パイ結合は、原子の半分満たされた原子軌道の横方向の重なりによって形成されます。
重なり合う軌道
シグマ ボンド: シグマ結合では、重なり合う軌道は次のようになります:2 つの混成軌道、または 1 つの混成軌道と 1 つの純粋軌道、または 2 つの純粋軌道
パイ ボンド: パイ結合では、重なり合う軌道は常に 2 つの純粋な (つまり、ハイブリダイズしていない) 軌道です。
存在
シグマ ボンド: シグマボンドは独立して存在します。
パイボンド: パイ結合は常にシグマ結合と共に存在します.
2 つの炭素原子の回転
シグマ ボンド: シグマ ボンドは自由な回転を可能にします。
パイボンド: パイ結合は自由回転を制限します。
絆の強さ
シグマ ボンド: シグマ結合は、パイ結合よりも強力です。
パイボンド: パイ結合はシグマ結合よりも強度が低くなります。
絆形成命令
シグマ ボンド: 原子が近づくと、シグマ結合が最初に形成されます。
パイボンド: パイ結合の形成の前に、シグマ結合が形成されます。
債券数
シグマ ボンド: 2 つの原子間にはシグマ結合が 1 つしかありません。
パイボンド: 2 つの原子間に 2 つのパイ結合が存在する可能性があります。
多原子分子における幾何学の制御
シグマ ボンド: 多原子分子の幾何学的制御には、シグマ結合のみが関与しています。
パイボンド: Pi 結合は、多原子分子の形状の制御には関与しません。
二重結合の結合数
シグマ ボンド: 二重結合には 1 つのシグマ結合があります。
パイボンド: 二重結合には 1 つのパイ結合しかありません。
三重結合の結合数
シグマ ボンド: 三重結合にはシグマ結合が 1 つあります。
パイボンド: 三重結合には 2 つのパイ結合があります。
電荷の対称性
シグマ ボンド: シグマ結合は、結合軸を中心に円柱電荷対称性を持っています。
パイボンド: パイ結合には対称性がありません。
反応性
シグマ ボンド: シグマ結合はより反応的です。
パイボンド: パイ結合は反応性が低いです。
形状決定
シグマ ボンド: 分子の形はシグマ結合によって決まります。
パイボンド: 分子の形はパイ結合では決まらない.
まとめ
シグマとパイは、2 つの原子軌道が重なったために形成される 2 種類の結合です。 2 つの原子の軸方向の重なりはシグマ結合を形成し、2 つの原子軌道の横方向の重なりはシグマ結合を形成します。これがシグマ結合とパイ結合の主な違いです。シグマ結合は常に最初に形成され、パイ結合よりも強力です。単結合は常にシグマ結合ですが、二重結合と三重結合にはシグマ結合と一緒にそれぞれ 1 つと 2 つのパイ結合があります。
参考文献
1. MOHAPATRA, R. K. (2014). エンジニアリング ケミストリー フォー ディプロマ . PHI ラーニング Pvt.
2. Srivastava, A. K. (2002). 簡単にできる有機化学 . New Age International.
3. Jespersen, N.D., &Hyslop, A. (2014). 化学:物質の分子的性質:物質の分子的性質. ワイリー グローバル エデュケーション。