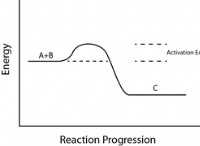
溶液 (酢や漂白剤など) の酸性度を測定するために使用される pH スケールについて聞いたことがあるでしょう。おそらく、酸は酸っぱいものであり (たとえば、クエン酸は酸っぱいキャンディーの一般的な成分です)、時には危険です (ほとんどの人は、大人になる前に「酸」という言葉を「潜在的な皮膚損傷」と関連付けることを学びます。ハリウッド映画や悲惨なニュース報道から)。
しかし、化学的に言えば、酸とは何ですか?また、溶液に溶解している酸のモル濃度がわかっている限り、溶液の pH を簡単に測定できるようにするさまざまな酸の個々の特性はありますか?その「署名」特性は酸解離定数と呼ばれます K
溶液中の酸
酸は、水溶液中でプロトン (まれに、連続して複数のプロトン) を供与できる分子です。つまり、水に溶解すると、イオン化されます。これは、プロトン (H) が水分子の間で「浮遊」することを意味し、多くの場合、ヒドロニウム イオンとして表されます。 (H3 O) これらの寄付された陽子を受け入れる水の能力のため.後に残る分子は陰イオンです。
例:炭酸 (H2 CO3 ) は、水溶液中でプロトンを供与して H になります (しばしば H
塩酸 (HCl) などの強酸は、はるかに多くの弱酸よりも「積極的に」プロトンを供与します。つまり、低 pH 環境、つまり、すでにプロトンが豊富で、それ自体が「積極的ではない」環境でもプロトンをオフロードできます。 「もっと取り上げる。弱酸は、周囲の pH が高い場合、つまりプロトン濃度が比較的低い場合にのみ、積極的にプロトンを提供します。
pH スケールとは?
上で、pH が低いということは、親酸から解放された多くのプロトンがある環境を意味することを読みました.たまたま、pH スケールは対数または「対数」スケールであり、実際には 1 から 14 の範囲で、最も酸性度の高いものから最も酸性度の低いものまでの範囲です。 pH の式は次のとおりです。
pH =-log_{10}[H^{+}]ここで、[H+] は陽子のモル濃度 (つまり、溶液 1 リットルあたりのモル数、または個々の原子/分子) です。プロトン濃度が 10 倍になるごとに、pH が低下します。 1 つの整数単位で、逆に。
例: 陽子の 0.025 M 溶液の pH はいくつですか?
pH =−log10 [0.025 mol/L] =1.602
酸イオン化定数 Ka
各酸には独自のイオン化定数があり、次の式で与えられます:
K_{a} =\dfrac{[A^{−}][H_{3}O^{+}]}{[HA]}
ここで[A]、[H3 O] と [HA] は、それぞれ、イオン化された酸、プロトン、イオン化されていない (つまり、「そのままの」) 酸の平衡濃度を表します。 K
pKa からの pH の計算:ヘンダーソン-ハッセルバッハの式
酸の pKa と上記の濃度から溶液の pH を計算できます。これは、供与されたプロトンを除外したものです。 pK
導出が含まれますが、Henderson-Hasselbach 方程式 これらの量を次のように関連付けます:
pH =pKa + log_{10}\dfrac{[A^{-}]}{[HA]}
例: K
解決するには、まず pKa を決定します。これは単純に −log10 です (1.77 × 10) =4.75。次に、[A] と [HA} の比率 =1/10 =0.1 という事実を使用します
pH =4.75 + log10 (0.1) =4.75 + (−1) =3.75
これは、酢酸の pKa よりも低い pH では、半分未満が解離またはイオン化されることを意味します。より高い pH 値では、半分以上がイオン化されます。実際、[A −] =[HA] と設定すると、酸の pKa は単に、酸の半分が解離し、半分が「無傷」である pH であることがわかります。