コア コンセプト
このチュートリアルでは、経験式と分子式とは何か、分子式と経験式の違いについて学びます。また、分子式と実験式の間の変換方法も学びます。最後に、経験式を使用してデータを含む分子式を見つける方法を学びます。
他の記事で取り上げるトピック
- 分子/化合物
- 化学結合
- 構造異性体
- 構成比
- 利回りの計算方法
語彙
分子 :2つ以上の原子が結合してできた化合物
n 値: 分子式を得るために経験式を乗じた整数
分子式
分子式 特定の分子に存在する各原子の数を表します。基本的に、これは分子内にどの要素が含まれているか、およびそれぞれの要素がいくつあるかのリストです。
分子式は、分子の特性に関する有用な情報を提供できます。単純な分子を名前に加えて説明する最も一般的な方法です。
分子式は常に完全なストーリーを示すとは限りません。分子内の要素のアイデンティティと数のみをリストするため、構造があいまいになることがあります.一部の化合物は同じ分子式 (同じ原子を同じ量で持つことを意味します) を持ちますが、配置が異なります。式は同じでも、形状や原子間の結合が異なる化合物は、異性体と呼ばれます。
例:
C6 H12 O6 → フルクトース、グルコース、ガラクトースを表す分子式。
N2 O4 → 四酸化窒素を記述するために使用される分子式。
C5 H3 N3 → シアノピラジンの分子式。
経験式
経験式 相対を表します 分子内の元素の量。これは、正確を与える分子式とは異なる場合があります。 量。分子内のすべての元素の相対量を知ることは、分子式を決定するのに非常に役立つため、実験式は有用です。
分子内の各原子の真の数を決定するには、n 値を取得することが重要です . n値は、分子式を得るために実験式に掛けられる整数です。分子式と経験式は、分子式の原子の比率が最も単純である限り、同じになる場合があります。つまり、n 値が 1 の場合です。
例:
CH2 O → フルクトース、グルコース、ガラクトースの経験式を還元。
NO2 → 還元された四酸化窒素の経験式。
C5 H3 N3 → シアノピラジンの実験式と分子式は、原子の比率を単純化できないため、同じです。
何が違うの?
分子式はリストであることに注意してください。分子内にあるすべての原子を表します。分子式は、多くの設定で分子について伝達するために使用され、時には化合物の特性についての洞察を与えることができます.
経験式は必ずしもそうではない 分子内の各元素の原子数を教えてください。それらの間の比率のみを示します。経験式は主に実験設定で使用され、分子式への足がかりとして機能します。
まれに、経験式が単独で役立つ場合があります。たとえば、一部の有機化学者は、経験式から炭素対酸素比を使用して、化学物質の反応性をすばやく推定します。ただし、一般に、実験式は分子の特性を理解するのに役立ちません。場合によっては、経験式を分子式として扱うことさえできないことがあります。たとえば、ベンゼン (C6 H6 ) 実験式 CH を持っています。 CH は実際に存在する可能性のある分子ではありません。これは、経験式が何らかの情報を見つけるための便利なツールである一方で、それが表す化合物の挙動について結論を出すために使用すべきではないことを示しています.
例
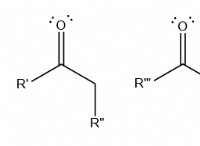
公式CH2を取る O.
まず、分子式として考えてみましょう。その式で分子を構築する方法は 1 つしかありません。その化学物質はホルムアルデヒドと呼ばれます。非常に有毒ですが、反応や防腐剤としても非常に役立ちます.
次にCH2について考えてみましょう 経験式としてのO。それはどのような分子式を表すことができますか?ホルムアルデヒド、酢酸 (酢)、乳酸 (細胞呼吸の重要な部分)、およびグルコースはすべて実験式 CH2 を共有します。 O.
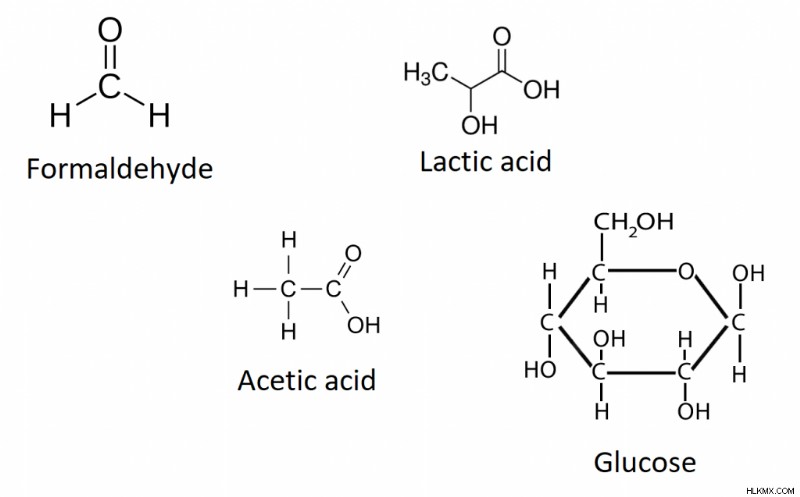
これらの分子は、単純な砂糖から危険な発がん物質まで、すべて非常に異なっています。それらはすべて同じ経験式を持っていますが、分子式と特性は大きく異なります。
分子式を実験式に変換する方法:
<オール>経験式を使って分子式を見つける方法
分子式から経験式を見つけるのは少し難しいかもしれませんが、その逆を行うのは非常に簡単です。経験式の各要素の添字に n 値を掛けるだけです。以下は質問の例です:
「実験式C3に対応する分子式は? H4 N2 n 値は 3 ですか?」
それを解決するために、各アトムの添字に n 値を掛けます。
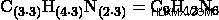
n値が指定されているのは奇妙に思えるかもしれません。答えを見つけるために n 値が必要な理由は、理論上、経験式 C3 を共有する分子式が無数にあるためです。 H4 N2 、n の値ごとに 1 つ。したがって、事前に「どこに行くのか」を知る必要があります。
データから分子式を見つける
一般に、実験データから分子式を見つける手順は次のとおりです。
<オール>練習問題 – 経験式の実験
以下は、経験式を使用して実験データで分子式を見つける方法の例です。
セットアップ
化学者が未知の化学物質の入ったキャニスターを受け取り、その分子式を解明する必要があります。彼女は、その化学物質に炭素と水素しか含まれていないことをすでに知っています.
研究者は未知の化合物の 50.0 グラムのサンプルを採取し、過剰な酸素ガスとの燃焼反応でそれを燃焼させ、CO2 を生成します。 と H2 O. 生成物を収集した後、彼女は反応が 156.8 g の CO2 を生成したことを発見しました および 64.2 g H2 O.
経験式を見つける
化学者は最初に各製品のモル数を見つけます:
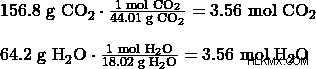
CO2 中のすべての炭素 は元の分子に由来し、水中のすべての水素と同様に、化学者はさらに次のことを発見しました:
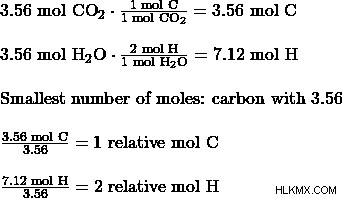
炭素の相対モル数は 1 で、水素の相対モル数は 2 です。これは、経験的 出発分子の式はCH2 .
分子式を見つける
さらにいくつかのテストを行った後、化学者は未知の化学物質の分子量が 42.09 グラム/モルであると結論付けました。彼女は経験的重み (つまり、化合物 CH2 の実験式の重み) を見つけます。 ) 1 モルあたり 14.03 グラムになります。定義上、n 値 実験式の倍は分子式に等しい。彼女はこの関係を使用して、次のことを見つけます。
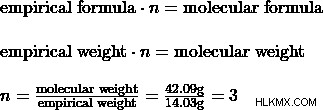
n 値が 3 の場合、化学者は実験式に 3 を「掛けて」分子式を求めます。
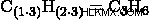
したがって化学者は、未知の化合物の分子式は C3 であると結論付けます。 H6 .
このチュートリアルの手順に従えば、経験式の問題は簡単に解決できるはずです。多くの化合物が同じ実験式を共有していることを忘れないでください。質量、物理的特性、反応性、およびその他の特性に基づいて違いを見つけることが、分子式を発見するための鍵となります.