化学式 H2O2 の場合、過酸化水素は水よりやや粘性があります。光の存在下では、不安定で分解可能です。人体にも存在する可能性があります。
重要な H2O2 のルイス構造は、分子の幾何学/形状、結合角を示します、ハイブリダイゼーション、およびその他のトピックについて説明します。 H2O2 は無極性か極性かなど。
H2O2 は、純粋な場合は苦味のある無色の液体です。酸素と酸素の結合が 1 つしかない、最も基本的な過酸化物です。 H2O2 は沸騰温度まで加熱されると非常に危険になり、爆発して重度の火傷を引き起こすことさえあります。
H2O2 の意味と重要性の構造を見てみましょう!
過酸化水素の有用な特性
• 強力な酸化剤です。
• 酸味があります。
• H2O2 は不燃性です。
• 融点は摂氏 0.43 度、沸点は摂氏 150.2 度です。
• 石油エーテルには不溶です。
過酸化水素の使用
• 皮膚の切り傷や火傷による感染を防ぐために使用されます。
• 医療機器の消毒に役立ちます。
• 冷蔵庫を掃除して食料を補充するため。
• 果物や野菜からほこりを取り除く。
• 消毒剤として機能します。
H2O2 のルイス構造をスケッチする最良の方法は何ですか?
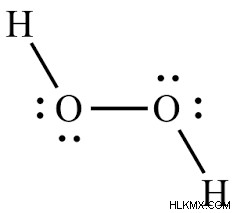
2 つの酸素原子と 2 つの水素原子が 2 つの O-H 結合と 1 つの O-O リンクを形成しますH2O2 のルイス構造。 H2O2 の意味のルイス構造では、4 つの孤立電子対と 3 つの結合対があります。
H2O2 の重要性を表すルイス ドット構造はかなり単純で、スケッチすると次のようになります。他の分子の描画に似ています。それでは、これを段階的に行う方法を見てみましょう.
いくつかの手順に従って、 H2O2 を描画します。 ルイスドット構造
H2O2 の価電子の総数を決定します。
最初のステップは、その中に価電子がいくつあるかを計算することです。それでは、水素と酸素の周期群を見てみましょう。
酸素は周期表の第 16 族に属しているのに対し、水素の原子価殻には 1 つの電子しかないため、その原子価殻には 6 つの電子があります。
酸素の価電子は6です
水素の価電子 =1
H2O2 のルイス構造を描くために利用できる価電子の総数 =12 + 2*6 =14
電気陰性度が最小の原子を中心に配置します。
水素が分子内に存在する場合、どの原子が多かれ少なかれ電気陰性であるかは問題ではありません。水素は常に分子の外側でルイス構造を形成し、原子価殻を完成させるのに 2 つの電子しか必要としません。
水素と酸素の間に単一のリンクを作成します。
水素と酸素を挿入したら、H2O2 の構造をさらに描くことができるように、それらを単結合で結合します。
外側の原子から始めて、残りの価電子を配置します。
ここで、外側の原子から始めて、残りの価電子を上記の構成に配置する必要があります。
ただし、H2O2 のルイス構造の外側の原子は水素であり、水素は原子価殻を完成させるために 2 つの電子しか必要としません。
H2O2 構造では、水素は酸素原子との単結合の助けを借りて、すでに 2 つの電子を共有しています。
その結果、残りの価電子が酸素の周りに配置され、オクテット規則が完成しました。
コア アトム オクテットを完成させ、必要に応じて共有結合を形成します。
これは、H2O2 のルイス構造を描く最後の段階です。このフェーズの酸素原子の周りに残りの価電子を配置して、オクテット規則を完成させます。
私たちには 8 個の価電子しか残っていないため、酸素は外殻を完成させるのに 8 個の電子を必要とします。さらに、単結合の助けを借りて、各酸素はすでに 4 つの電子を共有しています。
その結果、各酸素は 4 つの価電子だけでそのオクテットを完成させることができます。その結果、残りの価電子は酸素原子に配置されます。
H2O2 の分子構造とハイブリダイゼーションは何ですか?
過酸化水素 (H2O2) の分子構造は非平面分子です開いた本の構造を持つとも言われています。
VSEPR 理論によると、酸素原子上の孤立電子対は、別の原子の電子雲とできるだけ衝突して反発を減らします。その結果、無制限の電子対が隣接する結合対を押し下げます。
過酸化水素 (H2O2) ) 極性または非極性?
多くの人は、H2O2 が極性か非極性か確信が持てません。 H2O2 は分子構造が曲がっているため極性分子であり、コア原子 (酸素) に非共有電子対が存在すると電荷分布が不均等になり、極性になります。
結論
H2O2 は無色の液体で、多くの強度の溶液として作られ、主に綿やその他の織物、木材パルプの漂白、ロケット燃料としてのその他の化学物質の合成、化粧品や治療用途に使用されます。ただし、8% 以上の過酸化水素を含む溶液は皮膚に対して腐食性があります。