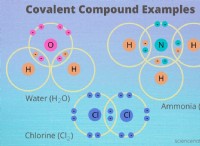
異性化とは、分子の化学式が同じでも構造が異なる現象です。さらに 2 つのカテゴリに分類できます。
- 構造異性:化学式が同じで中心金属との原子の結合が異なる分子を構造異性体と呼び、この現象を構造異性と呼びます。
- 立体異性:化学式が同じで、原子との結合が同じであるか、金属への配位子との配位が同じであるが、空間内の原子または配位子の空間配置が異なる分子を立体異性体と呼び、そのような分子を立体異性体と呼びます。を立体異性といいます。
立体異性体はさらに 2 つのカテゴリに分類できます:
<オール>光学異性
化合物は同じ化学式を持ち、配位子と金属との結合は同じですが、互いに鏡像を重ね合わせることができません。一般に、四面体および八面体の複合体で発生します。対称要素がないため、光学活性を示します。すべての正方形平面錯体はキラル配位子と配位しない限り対称面を有するため、正方形平面錯体は光学異性を示さない。光学異性体は、比回転などの立体化学的特性のみが異なる、融点、沸点、密度などの物理的特性を持っています。
<オール>光学異性体は、化合物の鏡像関係からエナンチオマーとジアステレオマーに分類できます。
エナンチオマーは、重ね合わせることができない鏡像を持つ立体異性体または光学異性体です。化合物の d および l 異性体はエナンチオマーと呼ばれます。
ジアステレオマーは、鏡像ではなく、重ね合わせることができない立体異性体です。幾何異性体はジアステレオマーです。
ラセミ混合物:2 つのエナンチオマー (左異性体と右旋異性体) の混合によって形成される等モル混合物です。
八面体複合体の光学異性:
- ML6 系の八面体錯体は、光学異性を示しません。それらは、対称面のため、光学的に不活性です (平面偏光を回転させることはできません)。 (M は金属、L は配位子)
- MA2B2C2 例:[Pt(py)2(NH3)2Cl2]
- M(AA)3 例:[Co(en)3]3+ M(AB) 3 (ABが二座配位子である)は、光学活性異性体を示す。例:[Cr(gly)3]
- 配位錯体の Mabcdef タイプには、15 の異性体が示されています。例えば。 [Pt(Cl)(Br)(I)(py)(NO2)(NH3)] は 15 の異性体を示します。これは、15 の異性体も鏡像を持っているためです。したがって、合計 30 の化合物が形成され、30 のすべてが光学活性になります。
四面体錯体における光学異性:
- ML4、ML3X、ML2X2 (L と X はどちらも単座配位子) タイプの四面体錯体は、対称面を含むため光学異性を持たず、光学的に不活性です。
- MABCD は対称面を持たないため、光学活性を示します。たとえば、Pt(NH3)(py)(Cl)(Br) は 2 つの光学異性を示します。
幾何異性
配位化合物は、化学式が同じで、中心金属との配位子の結合が同じですが、中心金属の周りの幾何学的配置が異なります。
この種の異性は、八面体および正方形の平面形状で見られますが、四面体複合体では他の配置が不可能であるため、四面体形状では見られません。これは、配位番号 4 と 6 を持つヘテロレプティック錯体で発生します。これは、中心金属の周りに配置が異なる可能性があるためです。
幾何異性体は、物理的および化学的性質が互いに異なります。
- ML4 タイプの四面体錯体は、すべての配位子が幾何異性の異なる方向にあるため、幾何異性を示しません。
- 八面体複合体の MA3B3 タイプは、面異性と経線異性を示します。
- MA2B2 タイプの正方平面複合体は、シスおよびトランス異性体を示します。シス異性体では、2 つの同じタイプの配位子の間の角度が 90° であり、トランス異性体では、2 つの同じタイプの配位子の間の角度が 180° です。
- 正方形平面複合体の MABCD タイプは、3 つの幾何異性体を示します。 2-cis および 1-trans.
- MA2B4 タイプの八面体複合体は、シス-トランス異性も示すことができます
- 面異性体および子午面異性体は、MA3B3 タイプの配位錯体です。フェイシャル異性体では、3 つの配位子がシス配置を持っていますが、メリディオナル異性体では、配位子の 1 つのペアがトランス配置になっています。たとえば、[RhCl3(pyr)3] は面異性と子午面異性を示します。
結論
立体異性とは、異性体の原子の空間配置が異なる現象です。立体異性は、光学異性と幾何異性に分類されます。光学異性体は対称要素のために光学的に活性ですが、幾何異性体は一般に対称面を含むため、一般に幾何異性体は光学的に活性ではありません。
エナンチオマーとジアステレオマーは、記事で例を挙げて説明されています。