ハロゲンは、周期表の第 7 族に属する元素です。ハロゲンファミリーには、フッ素、塩素、臭素、ヨウ素、アスタチン、およびテネシンが含まれます。ハロゲンは、電子を受け入れるための自由空間のために 1 の原子価を持っています。それらは、外殻に空孔があるため、非常に電気陰性です。ハロゲンは、それらの間に共有結合を持つハロゲン間化合物を形成するために、それ自体の中で反応する傾向があります.
そのような化合物の 1 つが五フッ化臭素です。五フッ化臭素のハイブリダイゼーションは、他の原子のハイブリダイゼーション プロセスと同様に、異なるエネルギーとさまざまな形状のハイブリッド軌道を形成します。
ハイブリダイゼーション:どういう意味ですか?
ハイブリダイゼーションとは一般に、2 つのものを混ぜ合わせることを意味し、ハイブリッドと呼ばれる新しい製品が生まれます。
化学では、混成とは、2 つの原子の軌道が混合して、親要素とは異なるエネルギー、形状、および特性を持つ新しい軌道を形成するという考えを指します。
ハロゲン
ハロゲンは、周期表の第 7 族の下に位置します。その名前は、塩を形成する性質を指します。ハロゲンファミリーには、F、Cl、Br、I、At、およびおそらく Ts が含まれます。
ハロゲンの性質
ハロゲンは、いくつかの一般的な物理的および化学的性質を持っています。通常は等核珪藻として存在します。
サイズ
グループの原子番号 9 の最初のハロゲンであるフッ素は、電子配置 2,7 の原子に 2 つの軌道を持っています。
グループを下に移動すると、原子に軌道が 1 つ追加されます。
したがって、ハロゲンのサイズはグループの下に向かって大きくなります。
価数
すべてのハロゲンは、原子価殻に電子を追加するための自由空間を持っています。
したがって、ハロゲンの原子価は常に 1 です。
電気陰性度
原子価殻に 1 つの電子を取り込む能力があるため、電気陰性度として作用します。
それらの電気陰性度特性は、下に移動するとサイズが大きくなるため、グループを減少させる傾向があります.
五フッ化臭素
五フッ化臭素 (BrF5) は、5 価の臭素原子によって形成されるハロゲン間化合物です。この分子は反応性が高く、蒸気の形をしているため、皮膚、目、粘膜を刺激します。
臭素の電子配置
臭素の原子番号は 35 です。
[Ar]4s23d104p5 の電子配置です。
フッ素の電子配置
フッ素の原子番号は 9 です。
電子配置は [He]2s22p5 です。
1 つのフッ素原子は、原子価殻から 1 つの電子対を失うと、臭素原子から 1 つの電子対を受け取ることができます。
したがって、5 つのフッ素原子が 5 価の臭素原子と結合し、ハイブリダイズした五フッ化臭素分子になります。
軌道内の電子
軌道は、電子が主に原子内に存在する 3D 空間です。通常、軌道は 2 つの電子を保持できます。
s 軌道は 2 つの電子を保持できます。
p 軌道は、px、py、pz に分割され、それぞれ 2 つの電子を含むため、6 つの電子を保持できます。
d 軌道は、dxy、dyz、dxz、dx2-y2、および dz2 に細分されるため、最大 10 個の電子を保持できます。
各軌道は 2 つの電子を保持します。したがって、合計で、d 軌道は最大 10 個の電子を保持します。
f 軌道は 14 個の電子を保持できます。
五フッ化臭素のハイブリダイゼーション
五フッ化臭素のハイブリダイゼーションにより、sp3d2 の軌道配置が得られます。
ハイブリダイゼーションにより、分子は四角錐形になります。
一般に、臭素の電子配置は 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p5 です。
しかし、5 価構造を実現するには、原子に 5 つの自由電子が必要です。
つまり、4p5 からの 3 つの電子が 4d 軌道にシフトし、5 つの孤立電子対になります。
シフトは 4p 軌道の半分満たされた構成を支持し、より安定させます。
また、4d 軌道の 5 つの軌道の 1 つを満たします。
したがって、5 つのフッ素原子は、臭素原子に結合した 1 つの孤立電子対を受け入れることができます。
したがって、それらの軌道はハイブリダイゼーションによって混合され、分子のハイブリッド形状を形成します。
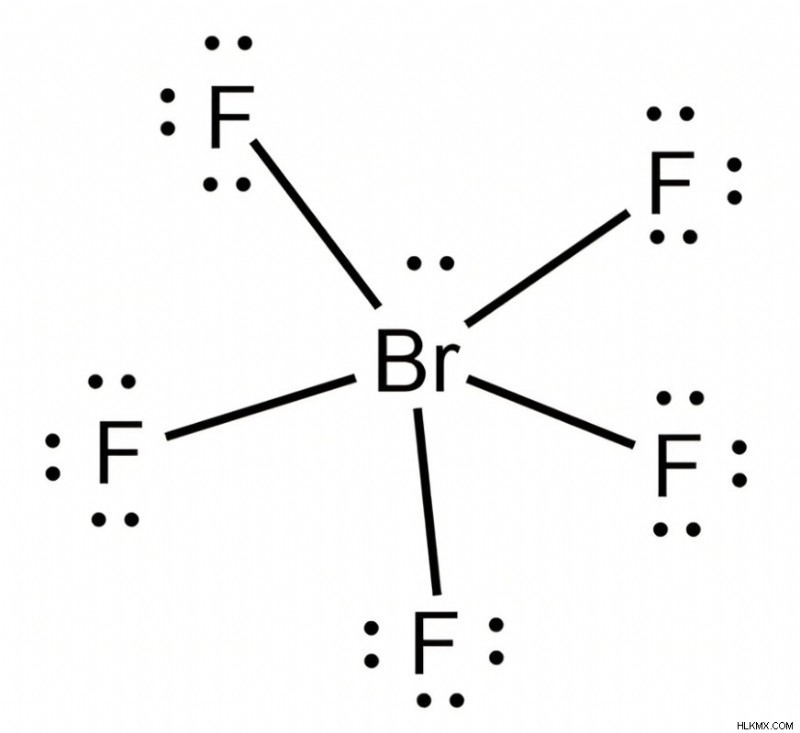
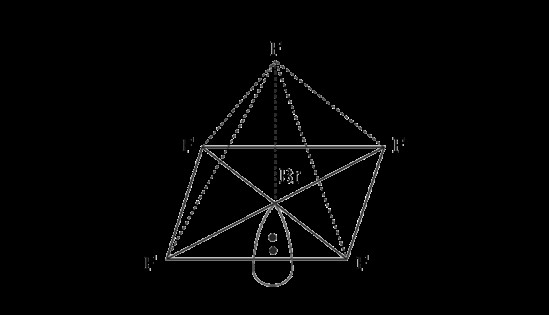
五フッ化臭素 – 四角錐構造
頭と頭を重ねると、五フッ化臭素はフッ素と 5 シグマ臭素結合を形成します。
中央の臭素原子には孤立電子対がまだ 1 つあります。
五フッ化臭素の用途
五フッ化臭素は刺激臭のある無色の液体です。
一般に、ロケット推進剤の酸化剤として機能します。
ウランを六フッ化ウランに変換する際に酸化剤の 1 つとして関与しています。
フルオロカーボンの合成に役立ちます。
結論
五フッ化臭素のハイブリダイゼーションは、五フッ化臭素という化学分子に関するすべての詳細を提供します。これは、5 価の臭素と 5 つのフッ素原子の間の共有結合により形成されたハイブリッド分子であり、1 組の電子が欠けています。反応性が高く、化学プロセスや商用ロケット推進剤で酸化剤として使用されます。
五フッ化臭素のハイブリダイゼーションは、sp3d2 ハイブリダイゼーションを形成し、四角錐の分子構造をもたらします。ハイブリッド分子は、共有電子の共有と約 90° の結合角のために 6 つのシグマ結合を持っています。ハイブリダイゼーションが発生するために、臭素の 4p 軌道からの 2 つの電子がその 4d 軌道にシフトします。