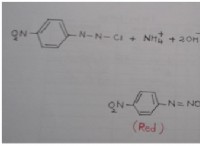
結合開裂または結合分裂は、化学結合の分割です。解離は、分子が 2 つ以上の成分に分解されるときに発生します。プロセスの性質に応じて、結合切断はホモリティックとヘテロリティックに分類できます。
シグマ結合の三重項励起と一重項励起のエネルギーは、それがホモリティック経路をたどるかヘテロリティック経路をたどるかを識別できます。金属-金属シグマ結合は例外です。結合の励起エネルギーが非常に高く、観察が不可能だからです。
結合切断タイプ
- ホモリティック分裂
- ヘテロリティック分裂
ホモリティック分裂
ホモリシスは、反応でフリーラジカルを生成します。

ホモリシスをサポートする要因は、ゼロまたは A と B の間の電気陰性度のわずかな変更です。つまり、μ =0 、𝚫EN =0 です。電気陰性度の差が小さいと、ホモリシス結合の切断によりラジカル中間結果が形成されます。ホモリシス結合の切断は、気相または非極性溶媒 (CCl4、CS2) の存在下で。熱分解を促進するために、紫外線、高温、または酸素のない高温などの特定の条件下で、この形態の結合切断が発生します。分子のホモリティック分裂に必要なエネルギー量は、ホモリティック結合解離エネルギーです。
ヘテロリティック結合分裂
ヘテロリシスでは、結合電子が 1 つのフラグメントに永久にシフトし、荷電フラグメントが (正および負) イオンを生成するような方法で結合が切断されます。

結合極性は、ヘテロリシスの背後にある主な理由です。より高い電気陰性度を持つ原子は、電子の結合対をそれ自体と保持する傾向があります。ヘテロリティック結合解離電気は、分子のヘテロリティック分裂に不可欠な強度の量です。
結合形成に関与する最も電気陰性度の高い (A) 原子を指す、結合の上に巻き毛の矢印を描くと、ヘテロリティック分裂が表されます。および H 原子との電子の結合ペアは、CH 結合のヘテロリティック分裂後に不均等に分布します。ここでは、C 原子と H 原子の電気陰性度が決定的な要因です。ポーリングによると、C の電気陰性度は 2.55、H の電気陰性度は 2.20 です。その結果、電子結合ペアは、電気陰性度の高い C に移動できます。
反応中間体
応答中間体は、多段階応答メカニズム内の一時的な種です。これは前のステップ内で生成され、後続のステップでフィードされて、長期的には最終的な応答成果物が生成されます。中間反応は、有機的な世界では珍しいことではありません。主要な例は、代謝産物と栄養代謝です。
有機反応の過程で形成される反応性、短寿命、高エネルギー、不安定な種は、反応中間体と呼ばれます。反応中間体は基本的に、反応の間に形成される種に関連しています。
カルボカチオン、カルバニオン、フリーラジカル、カルベン、ニトレンは反応中間体です。
例:A + B → C + D と仮定
上記の反応に含まれるステップは
A + B → X*
X* → C + D
ここで、化学種 X* は中間体です。
有機化学における反応中間体
- カルバニオン
有機化学では、さまざまな種類の反応中間体が存在します。カルバニオンは、炭素原子に恐ろしい料金がかかる自然化学反応中間体です。有機成分が完全に堅牢な塩基で処理されると、カルバニオンが形成されます。例は、ブタンと塩基の反応です。
カルバニオンは、底部がブタンから水素原子を除去するときに形作られます.
カルバニオンは非常に反応性が高く、化学反応で形成された後も長くは続きません。それらは通常、応答で幻想的な種と反応することにより、反応の停止生成物を生成するために交差します.これは、負に帯電した中間体を開発しているため、良い価格に引き上げることができるため、経験を積むことができます.
- フリーラジカル
もう 1 つの典型的な化学中間体はフリーラジカルです。固定されていないラジカルには、不対電子があります。電子で構成される共有結合が切断されると、各原子は結合電子の 1 つを受け取ります。メタンの炭素-水素結合が切断されると、結合の電子の 1 つが炭素に移動し、代替電子が水素に移動します。固定されていないラジカルを反映するために、小説が配置されている原子で単一のドットを使用します。
3.カルボカチオン
カルボカチオンは、炭素に正電荷を持っています。正に帯電したカルボカチオンは、最外殻に 6 個の電子しかありません。不完全なオクテットがあります。したがって、ルイス酸のように振る舞います。すべての電子が対になっているため、カルボカチオンは反磁性です。カルボカチオンは sp2 ハイブリダイズしています。カルボカチオンは平面です。カルボカチオンは、極性溶媒中で形成されます。電子供与基(EDG)の存在により安定化
結論
結合の切断は、結合切断として知られています。共有結合の電子は 2 つの原子間で、または原子間で同様に不均等に共有されるため、結合はホモリティックまたはヘテロリティックに損傷を受ける可能性があります。
電子を共有する 2 つの原子を含む共有結合は、有機分子の作成に広く使用されています。
共有結合を構成する原子は、次の 2 つの方法で分解できます。
ホモリティック分裂
ヘテロリティック分裂
ホモリティック分裂