ファン デル ワールス方程式のコア コンセプト
この記事では、非理想気体の状態を記述するために使用できる状態方程式の 1 つである ファン デル ワールスの方程式について学びます。 .
他の記事で取り上げるトピック
- シャルルの法則
- アボガドロの法則
- ボイルの法則
- 理想気体の法則
- 運動分子理論
ファンデルワールス方程式の紹介
おそらく学んだ気体の法則のほとんどは、理想気体にのみ適用されます。理想気体には、理想気体の法則に関する記事 理想気体の法則 で学ぶことができる一連の仮定が含まれます。 .ただし、これらの仮定は、発生する可能性のある一部のガスには実際には当てはまりません。それでは、ファン デル ワールスの方程式について学びましょう。
気体が理想的であるためには、圧力が低くなければならず、理想的には大気圧に近く、気体粒子の体積がシステムの体積と比較して無視できるようになります。
さらに、ガス粒子の運動エネルギーが分子間力の影響を大きく受けないように、温度を高くする必要があります。低温では、分子間力が粒子の運動により大きな影響を与えますが、運動エネルギーが増加するにつれて、影響は減少します。
補正係数
理想気体の範囲外の圧力と温度の範囲では、それらを考慮するために理想気体の式に補正係数を追加する必要があります。
最初の補正係数は、実在気体が占める体積を考慮することです。コンテナの全体積を考慮すると、ガスの体積がコンテナから取り除かれます。したがって、方程式に補正係数を追加できます。
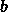
どこ  はガスのモル体積であり、
はガスのモル体積であり、 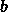 は、1 モルのガスが占める体積です。
は、1 モルのガスが占める体積です。
追加する 2 番目の補正項は、圧力を加えることによる分子間相互作用です。方程式を次のように書き直すことができます:
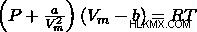
これはファン デル ワールスの状態方程式であり、この例のように理想的でない気体にも使用できます。他にも状態方程式があり、使用する状態方程式は状況によって異なります。