アミンは、すべての生物の非常に重要な構成要素であると考えられています。これは主に、世界中のすべての生物に不可欠なアミノ酸の生成を助けるためです.現在のエッセイでは、アミンの塩基性のさまざまな側面が提示され、議論されており、アミンがどのように機能するかをよりよく、完全かつ効果的に理解するのに役立ちます.ここでは、アミンの基本的な定義と説明を、その例と重要な傾向を含めて紹介しました。これにより、読者はアミンの塩基性をより適切に理解できるようになります。
アミンとは?
アミンは、アンモニアに由来する有機分子の一種として定義されます。アミンには、腐った魚のにおいに似た不快で独特のにおいがあります。ただし、臭いは非常に悪いですが、生命の生存に不可欠であることに注意する必要があります。アミンは、生きたタンパク質の構築を助けるアミノ酸の生成を助けます。さらに、生命を維持するために重要な物質もアミンによって多く出てきます。
アミンは、単一の窒素原子を中心とする分子です。この窒素は、2 つの水素原子と他の原子の 1 つのグループに接続されています。このため、アミンは地球上のあらゆる生物にとって非常に重要です。ただし、1 つまたは両方の水素原子は、原子の任意のグループで簡単に置き換えることができますが、分子は依然としてアミンとして分類されます。
アミンの塩基性
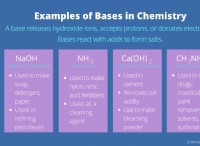
アミンは窒素原子の孤立電子対で構成されているため、この化合物は塩基性で良好な求核剤になります。アミンの塩基性は、N 原子上の孤立電子対を供与する能力として定義できます。これにより、アミンはそのペアを電子不足の中心に簡単に寄付できるため、「塩基性」になります.アミンは、sp3 ハイブリダイゼーションのために四面体の形状を持つ傾向があります。この場合、ライン ペアは混成軌道の 1 つにあります。したがって、アミンの塩基性は、気体状態と水性状態の両方の場合で研究および評価できますが、異なる要因が両方の状態に影響を与えます。
アミンは弱塩基を持っています。したがって、アミンの塩基性の相対性は、それぞれの共役酸の pKa 値で簡単に比較できます。この点で、第一級アルキルアミンはアンモニアよりも基本的であると言えます。ここで、アルキル基はアルキルアンモニウムイオンの安定化に役立つ傾向があることに注意することが不可欠です。
アミンの塩基性の例
アミンには、第一級、第二級、第三級の 3 種類があります。第一級アミンは、R で表されるアルキル基がアンモニアの 3 つの水素の 1 つを置き換えるときに発生します。これは、芳香族かどうかに関係なく、炭素鎖を示します。炭素鎖に結合した NH2 の存在によって、その構造が定義されます。第一級アミンの例のいくつかには、エチルアミンおよび2-メチル-プロパン-1-アミンのようなものが含まれる。 2級アミンは、アンモニアの2つの水素原子がR基と交換されるときに発生します。二級アミンの例は、エチルメチルアミンおよびジエチルアミンである。トリメチルアミンおよびトリフェニルアミンは、第三級アミンの例の一部です。
アミンの主な塩基性傾向
アミンは、主にすべての生物に不可欠なアンモニア酸の生成を助けるため、生命の不可欠な構成要素です。アミンの塩基性に関しては、いくつかの傾向があります。それらは次の点でリストされ、提示されます:
- 窒素の負電荷が増加すると塩基性が増加します
- 共鳴、または共役アミンと非共役アミン
- 誘導効果により塩基性が低下
- π受容体とπ供与体
- ハイブリダイゼーション
塩基性が電子対の不安定性として大まかに解釈できる場合、不安定性は電荷の密度とともに増加することに注意する必要があります。その結果、塩基性度は、負電荷の増加とともに増加するはずです。アミンの共役塩基は、常にアミン自体よりも強い塩基であると言えます。
結論
アミンは、すべての生物の非常に重要な構成要素であると考えられています。これは主に、世界中のすべての生物に不可欠なアミノ酸の生成を助けるためです.現在のエッセイでは、アミンの塩基性のさまざまな側面が提示され、議論されており、アミンがどのように機能するかをよりよく、完全かつ効果的に理解するのに役立ちます.アミンは、単一の窒素原子を中心とする分子です。アミンは弱塩基を持っています。第一級アルキルアミンは、アンモニアよりも塩基性が高くなります.