硫酸(H2SO4)と水およびアルコール化合物との反応により、熱が発生します。硫黄、酸素、水素からできています。多くの産業では、化学化合物を鉱石の処理や肥料の製造などに使用しています。無色無臭の液体は、水、砂糖、亜鉛などの金属と反応し、さまざまな生成物を生成します。その広大な産業用途に続いて、化合物は廃水からの悪臭の処理においてユーザーに利益をもたらします.また、化学薬品によるポリマーなどの固体粒子の除去にも役立ちます。化学物質はいくつかの点で有利であるため、適用目的で特定の反応性化合物を受けます。反応と実験はしばしば危険であり、爆発につながります。研究所は時々それらを専門的なビジョンの下で運びます。それでは、概念について簡単に説明し、同時にその反応を学びましょう.
硫酸とは?
硫酸は、商業目的で広く使用されている化合物です。水と三酸化硫黄と反応して生成する無色無臭の液体です。さらに、化学物質は、ガソリン精製や冶金などのさまざまな産業によって占められています。多くの場合、適用プロセスで酸蓄電池の電解質として機能します。
硫酸の作り方
次の簡単な手順に従って硫酸を調製できます-

硫酸の反応は?
硫酸と化合物との反応は非常に発熱的です。以下の硫酸の4つの重要な反応を読んでください-
- 硫酸と水との反応
- 糖と硫酸の反応
- 硫酸と亜鉛の反応
- 硫酸とバリウムの反応
硫酸と水の反応 (H₂ O)
硫酸と水との反応 は、発熱プロセスを引き起こします。化学化合物、つまり三酸化硫黄が水 (H2O) と反応すると、その露出からかなりの量の熱が放出され、場合によっては沸騰することさえあります。化学実験を行っている間、安全なプロセスを確実にする唯一の方法は、他の方法や技術ではなく、水に硫酸を加えることです.
脱水性硫黄物質は、反応でいくつかの化合物から水を押し出し、次に溶液を乾燥剤として使用します。ただし、この化学反応の沸点は濃度レベルに依存し、全体で 98% にまで及びます.
場合によっては、発煙硫酸 (SO3 溶液) の三酸化硫黄濃度が高いために沸騰が低下します。
硫酸と糖の反応
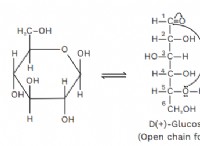
硫酸と糖の反応 硫酸と水の化学的関係は、古典的な実験で糖化合物、つまり炭水化物を追加することによって実証されます。硫酸の反応 は、物質から水を分離する傾向があるため、その過程で分子を破壊するのに役立ちます.ただし、以下の手順は慎重に行ってください-
ステップ 1:ボウルに砂糖を入れ、水滴を加えて混ぜます。
ステップ 2:混合物に硫酸を加えます。
数分後、強い反応が起こり、ガス、二酸化炭素、二酸化硫黄が同時に放出されます。現在、硫酸と砂糖の化学反応が盛んに行われています。将来のためにこの実験を書き留めておくことができます。
硫酸と亜鉛の反応
硫酸と亜鉛の化学反応は、他のすべての実験によく見られます。多くの場合、プロセスで水素ガスを生成するために、反応は実験室で広くカスタマイズされています。さらに、亜鉛粒に希硫酸を加えると、その過程で水素ガスを放出しながら金属物質を完全に溶解します。反応から得られる式は
Zn + H₂ SO4 → ZnSO4 + H₂
その後、希硫酸は水素ガスの活性で反応する金属と反応を形成します。式は –
М + H₂ SO4 (希釈) → 塩 + H₂ ↑
硫酸と塩化バリウムの反応
バリウムは塩化物陰イオンとバリウム陽イオンからできた塩です。したがって、硫酸と塩の間の反応はバリウムイオンを形成します。反応中、陰イオンがプロセスに表示され、それが新しい化合物の形成につながります。硫酸はルイス酸として作用し、実験では白色を形成します。以下は、実験を完了した後に得られた式で、重量測定でよく使用されます。
H₂ SO4 + BaCl₂ → BaSO4 + 2HCl
ZnSO4 + BaCl₂ → BaSO4 + 塩化亜鉛₂
実験では、硫酸はさまざまな化合物や塩から金属を置換できる最も強力な化学物質です。
結論
硫酸は、工業目的に機能する不可欠な商品です。病原体の悪臭を除去するのに役立つため、多くの業界でこの化合物が広く使用されています。実験室では、三酸化硫黄と発煙硫酸の混合物を使用して硫酸を調製し、幅広い用途に供給しています。ただし、特定の化合物は硫酸と反応して価値のある化合物を形成します。硫酸は、製造工程後の洗浄剤として機能します。その多くの用途に続いて、化合物は「化学物質の王様」として知られています。