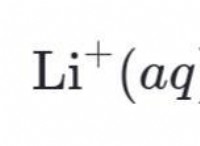主な違い – 酸塩基滴定と酸化還元滴定
滴定は、濃度による化学分析物の定量化に広く使用されている実験技術です。これは、一連の特別な装置を使用して実行されます。一般に、それは正体がわかっている 2 つの液体溶液間で実行されます。 (ほとんどの場合) 検体の濃度である未知のパラメーターを見つけるには、他の溶液の濃度を知る必要があります。プロセスの混乱を避けるために、ソリューションは異なる名前でラベル付けされ、それぞれの装置に配置されます。したがって、既知の濃度の溶液は「滴定液」と呼ばれます '、そして通常はビュレットに入れられます。未知の濃度の溶液/調査中の溶液は「タイトランド」と呼ばれます 'または分析物であり、通常は滴定フラスコに入れられます。滴定の当量点を見つけるために化学指示薬がよく使用され、通常、指示薬は滴定フラスコ内の溶液に添加されます。インジケーターは、それが入っている媒体に敏感で、それに応じて色を変えることができます。これはあらゆるタイプの滴定の基礎です .滴定には主に酸塩基滴定と酸化還元滴定の 2 種類があります。 主な違い 酸塩基滴定と酸化還元滴定の違いは、酸塩基滴定には酸と塩基が含まれることです。 一方、レドックス滴定には 2 つのレドックス種が含まれます。
酸塩基滴定とは
これは、関与する 2 つの種が酸と塩基であるタイプの滴定です。 .種間の反応タイプは酸塩基中和反応であり、副生成物として水が形成されます。原則として、塩基は滴定フラスコに保持され、酸はビュレットに加えられます。 2 つの種の間で発生する反応は、H+ イオンと OH- イオンの間の反応にまで及びます。最後に採取するのはビュレットからの体積測定です。したがって、既知量の滴定液と完全に反応するために必要な滴定液の量が記録されます。これらの数値は化学量論と化学式に関連付けられ、未知の溶液の濃度を決定できます。
通常、滴定の当量点/終点を決定するために、酸塩基指示薬が滴定フラスコ内の塩基溶液に追加されます。酸塩基指示薬は、塩基性媒体で 1 つの色を示し、酸性媒体で別の色を示すことができます。完全に中和した後、ビュレットから滴定フラスコ内の塩基に酸を 1 滴追加すると、媒体は塩基性から酸性に変わります。指示薬の色も変わり、滴定が停止します。強酸を強塩基で滴定すると、当量点は pH=7 になりますが、使用する酸/塩基が弱ければ pH 曲線は変化します。

滴定メチル オレンジ
レドックス滴定とは
レドックス滴定は、滴定の一般的な構成に準拠する別のタイプの滴定です。ただし、この場合、2 つの種の間の反応は酸化還元反応です .これは、反応が酸化/還元反応の形をとり、一方の種が酸化され、もう一方の種が還元されることを意味します。そして、これがレドックス反応の実現可能性を決定します。特定の種が酸化されると、電子が放出され、酸化数が増加します。種が還元されると、電子を受け取り、酸化数が減少します。したがって、酸化還元反応では、循環する電子の量は一定のままです。つまり、酸化種によって放出された電子は、反応の化学量論に応じて、還元種によって受け入れられる必要があります。
一部の酸化還元種は、MnO4 などの自己指標として機能します Mn に還元されると紫色を失うイオン。その他の場合、I2 の反応など デンプンはヨウ素との複合体の形成により発色するため、インジケーターとして使用されます。一般に、Fe2+/Fe3+、Cr3+/Cr6+、Mn7+/Mn2+ などの「d」ブロック元素は、可変の酸化数を持つため、一般的に酸化還元反応に関与します。

終点前(左)と終点後(右)のヨウ素滴定混合物の色
酸塩基滴定と酸化還元滴定の違い
定義上
酸塩基滴定では、 関連する種は酸と塩基です。
レドックス滴定 酸化還元種間で行われる滴定です。
種間の反応
酸塩基滴定 、種は水分子を形成する中和反応に参加します。
レドックス滴定 、種は酸化および還元反応を通じて反応します
インジケーターの使用
弱酸と弱塩基は、酸塩基滴定の指標として使用されます。
一部の酸化還元種は自己指標として機能し、ほとんどの場合、特別な 酸化還元 インジケーターが使用されます。
発生
酸塩基滴定 あらゆる形態の酸と塩基/弱と強の間で発生する可能性があるため、より一般的です.
レドックス滴定 「d」ブロック要素の間でよく見られます。