主な違い – 脱水合成と加水分解
化学反応は、反応の性質に応じてさまざまなグループに分類できます。脱水合成と加水分解はそのような化学反応です。これらの反応は、そのメカニズムに従って分類されます。これらの反応はどちらも、水分子の合成または消費を伴います。脱水合成と加水分解の主な違いは、脱水合成では小さな分子から大きな分子が形成されるのに対し、加水分解では大きな分子から小さな分子が形成されることです。
対象となる主な分野
1.脱水合成とは
– 定義、メカニズム、例
2.加水分解とは
– 定義、メカニズム、例
3.脱水合成と加水分解の違いは何ですか
– 主な相違点の比較
重要な用語:カルボン酸、縮合、脱水合成、エステル化、グリコシド結合、加水分解、ペプチド結合

脱水合成とは
脱水合成は、水分子の放出を伴うより大きな分子の形成です。ここでは、2 つ以上の小さな分子が互いに共有結合を形成し、各結合ごとに水分子を放出します。したがって、脱水合成反応の最終生成物は、常に反応物よりも複雑な化合物です。脱水合成反応は、大きな分子が生成されるため合成反応の一種です。
これらの脱水合成反応は、縮合とは水分子の形成を指すため、縮合反応とも呼ばれます。したがって、水酸基 (–OH) を持つ分子と放出可能なプロトンの間で脱水合成が起こります。
化学合成プロセスでは、水分子を放出してより大きな分子を得るために脱水合成が使用されます。例えば、アルコールとカルボン酸との反応はエステルを生成し、副生成物として水分子を放出することがある。ここで、カルボン酸の-OH基が放出され、アルコールの酸素に結合した-H原子も放出されます。したがって、これら 2 つの –OH 基と –H 基が結合して水分子を形成します。
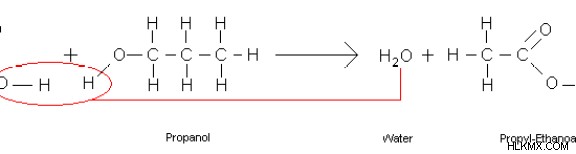
図 01:エステル化
生物学的システムでは、グリコシド結合とペプチド結合という用語は、分子間の結合を表すためによく使用されます。グリコシド結合は、水分子を放出する 2 つの単糖間の反応の結果として形成されますが、ペプチド結合は、水分子を放出する 2 つのアミノ酸間の反応の結果として形成されます。したがって、これらは縮合または脱水合成反応です。
加水分解とは
加水分解は、水の存在下で化学結合が切断されることです。ここで、水は反応プロセスに関与する反応物として機能します。加水分解反応では、大きな分子は常に小さな分子に分解されます。したがって、生成物とは異なり、反応物には常に複雑な分子が含まれます。これらの反応では、水分子が反応物分子に追加され、その反応物に存在する化学結合が切断されます。
大きな分子が加水分解されると、結果として得られる 2 つの小さな分子は、水分子から -OH 基と -H 基を取得します。加水分解は縮合の反対です。これは、縮合反応では水分子が形成されるのに対し、加水分解では水分子が消費されるためです。
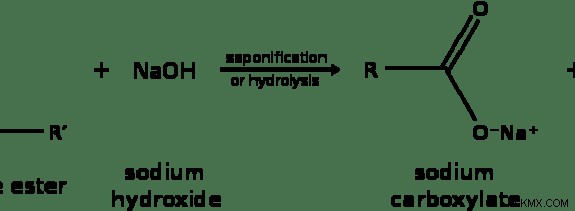
図 2:エステル加水分解反応
脱水合成反応と同じ例を挙げると、エステルの加水分解はエステル化反応の反応物を形成します。それらはカルボン酸とアルコールです。このために、ベースが使用されます。したがって、安定性が高いため、カルボン酸の代わりにカルボン酸イオンが形成されます。ただし、この反応は、カルボン酸形成のための-OH基とアルコール形成のための-H基を提供するために、水分子を消費します。このプロセスはけん化と呼ばれます。
脱水合成と加水分解の違い
定義
脱水症状: 脱水合成は、水分子の放出を伴うより大きな分子の形成です。
加水分解: 加水分解は、水の存在下での化学結合の切断です。
メカニズム
脱水症状: 脱水合成反応は複合反応です。
加水分解: 加水分解反応は分解反応です。
水分子
脱水症状: 脱水合成反応は水分子を形成します。
加水分解: 加水分解反応は水分子を消費します。
反応物
脱水症状: 脱水合成反応の反応物は、その生成物よりも小さな分子です。
加水分解: 加水分解反応の反応物は、その生成物よりも複雑な分子です。
副産物
脱水症状: 脱水合成反応は、副産物として水分子を生成します。
加水分解: 加水分解反応は副産物を与えません。
結論
脱水合成も加水分解も、水の存在下で起こる化学反応です。これは、脱水合成反応が媒体に水分子を提供するのに対し、加水分解反応は反応混合物から水分子を消費するためです。脱水合成と加水分解の主な違いは、脱水合成では小さな分子から大きな分子が形成されるのに対し、加水分解では大きな分子から小さな分子が形成されることです。