主な違い - 陽電子放出と電子捕獲
陽子と中性子の数が不均衡なために不安定な天然同位体がいくつかあります 彼らは原子核に持っています。したがって、安定するために、これらの同位体は放射性崩壊と呼ばれる自発的なプロセスを経ます。放射性崩壊により、特定の元素の同位体が別の元素の同位体に変換されます。陽電子放出、ネガトロン放出、電子捕獲など、さまざまな崩壊経路があります。陽電子放出は、放射性崩壊の過程で陽電子と電子ニュートリノが放出されることです。電子捕獲は、電子ニュートリノを放出するプロセスです。これらのプロセスは両方とも、陽子が豊富な原子核で行われます。 陽電子放出では、放射性核内の陽子が陽電子を放出しながら中性子に変換されます。電子捕獲では、中性原子の陽子が豊富な原子核が内殻電子を吸収し、それが陽子を中性子に変換して電子ニュートリノを放出します .これが陽電子放出と電子捕獲の主な違いです。
対象となる主な分野
1.陽電子放出とは
– 定義、原則、例
2.電子捕獲とは
– 定義、原理、例
3.陽電子放出と電子捕獲の類似点は何ですか
– 共通機能の概要
4.陽電子放出と電子捕獲の違いは何ですか
– 主な違いの比較
重要な用語:原子、電子、電子ニュートリノ、原子核、中性子、陽電子、陽子、放射性崩壊

陽電子放出とは
陽電子放出は、放射性核内の陽子が陽電子と電子ニュートリノを放出しながら中性子に変換される放射性崩壊の一種です。これは、ベータ + 減衰とも呼ばれます .陽電子は、電子と同じ質量を持ち、数値的には等しいが正の電荷を持つ亜原子粒子です。ベータ粒子(βまたはe+)とも呼ばれます。電子ニュートリノ (Ve) は、正味の電荷を持たない素粒子です。陽電子放出は、陽子が豊富な放射性核で発生します。
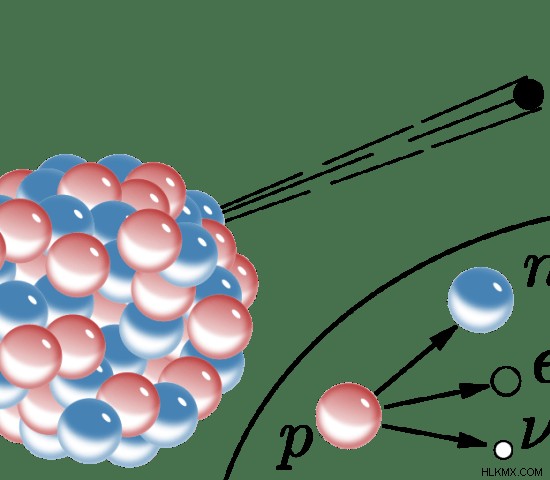
図 1:図での陽電子放出
陽電子放出では、原子核の原子番号が 1 減ります。原子の原子番号は、原子核に存在する陽子の総数です。しかし、陽電子放出では、これらの陽子の 1 つが変換されます。原子番号の減少を引き起こします。ただし、原子の質量数は変わりません。これは、陽子が中性子に変換され、質量数が原子内の陽子と中性子の合計になるためです。次の核反応は、陽電子放出の一例です。
6 C → 5 B + e + V + エネルギー
これは炭素の同位体です。炭素の放射性同位体です。それは陽電子放出を介してホウ素-11に崩壊します。ホウ素 11 は、ホウ素の安定同位体です。
電子捕獲とは
電子捕獲は、原子核が内殻電子を吸収し、陽子を中性子に変換して電子ニュートリノとガンマ線を放出する一種の放射性崩壊です。このプロセスは、陽子が豊富な原子核で行われます。内殻電子は、原子の内部エネルギー準位からの電子です (例:K 殻、L 殻)。同時に、このプロセスは電子ニュートリノの放出を引き起こします。プロセスの核反応は次のように与えられます。
P + e → n + Ve + γ
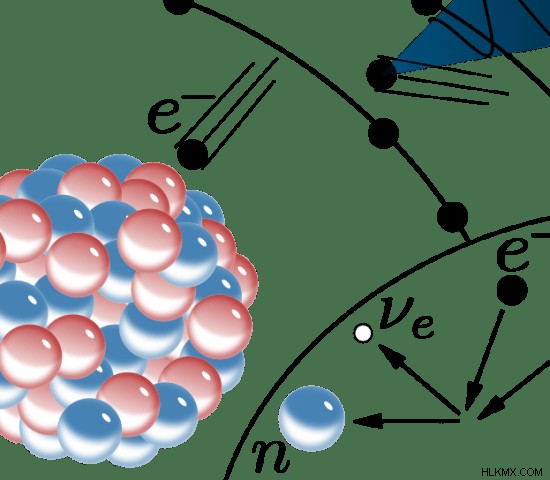
図 2:電子捕獲の原理
原子番号は原子核内の陽子の総数であり、このプロセスで陽子は中性子。ただし、質量数は変わりません。電子捕獲は電子殻の電子の損失をもたらすため、陽子 (正電荷) の損失によってバランスがとられ、原子は電気的に中性のままになります。
N7 + e → C6 +ベ+γ
上記の反応により、窒素同位体の電子捕獲が得られます。電子ニュートリノとガンマ線とともに炭素13原子を形成します。炭素 13 は、炭素の天然の安定同位体です。
陽電子放出と電子捕獲の類似点
- どちらも放射性崩壊の形態です。
- どちらの形態も陽子が豊富な環境で発生します
- どちらも電子ニュートリノを放出します。
- どちらの形式も、原子番号または原子の質量数を変更しません。
陽電子放出と電子捕獲の違い
定義
陽電子放出: 陽電子放出は、放射性核内の陽子が陽電子と電子ニュートリノを放出しながら中性子に変換される放射性崩壊の一種です。
電子捕獲: 電子捕獲は、原子核が内殻電子を吸収して陽子を中性子に変換し、電子ニュートリノとガンマ線を放出する一種の放射性崩壊です。
排出量
陽電子放出: 陽電子放出は、電子ニュートリノとともに陽電子を放出します。
電子捕獲: 電子捕獲は、電子ニュートリノとガンマ線を放出します。
原則
陽電子放出: 陽電子放出は、陽子から中性子、陽電子、電子ニュートリノへの変換として発生します。
電子捕獲: 電子捕獲は、内殻電子を吸収することにより、陽子が中性子と電子ニュートリノに変換されることで発生します。
結論
特定の元素の不安定同位体の放射性崩壊は、その同位体を別の化学元素の別の同位体に変換します。いくつかの腐敗経路があります。陽電子放出と電子捕獲は、そのような経路の 2 つです。陽電子放出と電子捕獲の主な違いは、陽電子放出では、放射性核内の陽子が陽電子を放出しながら中性子に変換されるのに対し、電子捕獲では、中性原子の陽子に富む核が内殻を吸収することです。電子ニュートリノを放出する中性子に陽子を変換します。
参照:
1.ヘルメンスティン、アン・マリー。 「電子捕獲の定義」 ThoughtCo、2014 年 6 月 25 日、こちらから入手可能。
2.「崩壊経路」。 Chemistry LibreTexts、Libretexts、2017 年 6 月 10 日、こちらから入手可能。
画像提供:
1. Master-m1000 による「Beta-plus Decay」 – Inductiveload (パブリック ドメイン) による Beta-minus Decay.svg に基づく自身の作品
2. Master-m1000 による「Electron capture」 – および自己-作る。このベクター画像は、コモンズ ウィキメディア経由で Inkscape (パブリック ドメイン) で作成されました