主な違い 逆相クロマトグラフィーと疎水性相互作用クロマトグラフィーの違いは、逆相クロマトグラフィー (RPC) はより疎水性の高い媒体を使用するため、相互作用がより強くなるのに対し、疎水性相互作用クロマトグラフィー (HIC) は、逆相クロマトグラフィー .
逆相クロマトグラフィーと疎水性相互作用クロマトグラフィーは、クロマトグラフィー媒体の疎水性表面と生体分子表面の疎水性パッチとの間の相互作用に依存する 2 つのクロマトグラフィー技術です。
対象となる主な分野
1.逆相クロマトグラフィーとは
– 定義、手順、適用
2.疎水性相互作用クロマトグラフィーとは
– 定義、手順、適用
3.逆相クロマトグラフィーと疎水性相互作用クロマトグラフィーの類似点は何ですか
– 共通機能の概要
4.逆相クロマトグラフィーと疎水性相互作用クロマトグラフィーの違いは何ですか
– 主な相違点の比較
主な用語
疎水性相互作用クロマトグラフィー、HIC、メディア、逆相クロマトグラフィー、RPC
逆相クロマトグラフィーとは
逆相クロマトグラフィー (RPC) は、タンパク質、ペプチド、オリゴヌクレオチドなどの生体分子の精製と分析に使用されるクロマトグラフィー技術です。高分解能の分離が可能で、ペプチド マッピングや純度チェックに最適です。 RPC は、ペプチドおよびオリゴヌクレオチドの最終研磨でより頻繁に使用されます。
2 種類の主な疎水性媒体を固定相として使用できます:炭素鎖で覆われたシリカ ビーズまたは裸の疎水性ポリマーです。カラムには疎水性媒体が充填層の形で充填され、その上にサンプルが適用されます。トリフルオロ酢酸 (TFA) などのイオンペア剤を移動相に添加して、疎水性相互作用の形成を強化することができます。 5% アセトニトリルなどの有機修飾剤を最初に使用し、アセトニトリルの % を増やすことで溶出を開始できます。
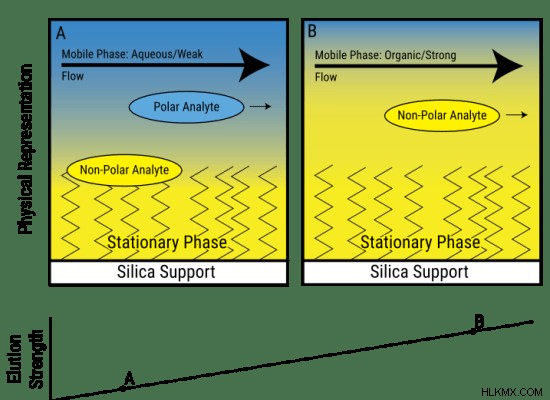
図 1:逆相クロマトグラフィーの理論
疎水性が低い/極性が高い生体分子が最初に溶出し、疎水性が高い分子は後で溶出します。 RPC は、分離能が最も高いクロマトグラフィー技術です。
疎水性相互作用クロマトグラフィーとは
疎水性相互作用クロマトグラフィー (HIC) は、適度な条件下での疎水性に基づく生体分子の分離に使用されるもう 1 つの手法です。これは、サンプルを最初のサンプル濃縮およびクリーンアップで硫酸アンモニウム沈殿に供する必要がある場合に、タンパク質の精製に理想的な手法です。硫酸アンモニウム沈殿中の塩レベルの上昇により、疎水性成分間の相互作用が増加します。
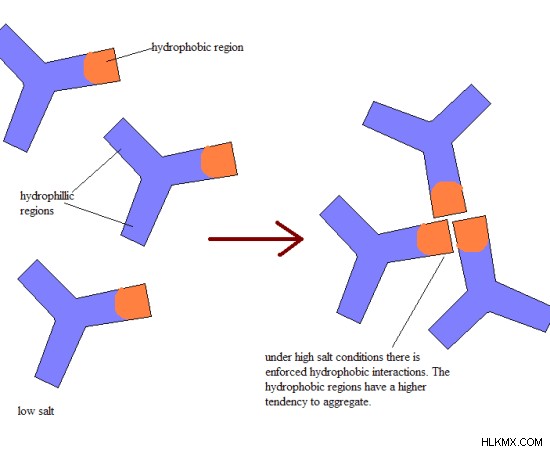
図 2:疎水性相互作用に対する高塩濃度の影響
HIC の疎水性媒体は、アルキル基またはアリール基を含む配位子でコーティングされた球状粒子の不活性マトリックスで構成されています。疎水性相互作用は、適度に高い塩濃度 (通常は 1 ~ 2 M 硫酸アンモニウムまたは 3 M NaCl) で発生します。開始バッファーは、不純物を洗い流しながら、目的のタンパク質が培地に確実に結合するようにします。溶出バッファーには低塩濃度が含まれており、タンパク質と固定相の間の相互作用が弱まっています。
逆相クロマトグラフィーと疎水性相互作用クロマトグラフィーの類似点
- 逆相クロマトグラフィーと疎水性相互作用クロマトグラフィーは、疎水性に基づく生体分子の分離に使用される 2 つの技術です。
- 両方の技術の移動相は、水または有機溶媒です。
- 充填層カラムを使用しています。
- 開始バッファーにより、目的の分子がカラムに確実に結合します。
- 疎水性が最も低い分子が最初に溶出し、より疎水性の高い分子が後で溶出する場合があります。
- 最後の洗浄ステップでは、最も強く結合した分子が溶出されます。
- 両方の技術の分解能は、選択性 (ピーク間の分離の程度)、技術の効率 (狭く対称的なピークを生成する能力)、サンプルの質量、および保持時間の組み合わせです。
逆相クロマトグラフィーと疎水性相互作用クロマトグラフィーの違い
定義
逆相クロマトグラフィー (RPC) は、混合物中の分子の疎水性に基づく最高分解能の分離技術を指し、疎水性相互作用クロマトグラフィー (HIC) は分離技術の一種を指します。疎水性に基づいていますが、比較的穏やかな条件下で動作します。
疎水性
RPC はより疎水性の高い条件下で動作しますが、HIC は比較的穏やかな疎水性の条件下で動作します。
交流
逆相クロマトグラフィーは、有機修飾剤による溶出中に逆にする必要がある分子と固定相の間のより強い相互作用につながりますが、HIC は固定相と
疎水性メディア
RPC は、炭素鎖で覆われたシリカ ビーズまたは裸の疎水性ポリマーを使用しますが、HIC は、アルキルまたはアリール基を含む配位子でコーティングされた球状粒子の不活性マトリックスを使用します。
開始バッファー
RPC の開始バッファーはトリフルオロ酢酸 (TFA) を使用しますが、HIC の開始バッファーは適度に高い塩濃度を使用します。
溶出
アセトニトリルの割合が増加すると RPC で溶出が始まり、塩濃度が減少すると HIC で溶出が始まります。
解決策
逆相クロマトグラフィーは分離度が最も高いクロマトグラフィー技術ですが、HIC の分離度は RPC に比べて低くなります。
アプリケーション
RPC はタンパク質、ペプチド、オリゴヌクレオチドの分離に使用され、HIC は主にタンパク質の精製に使用されます。
結論
逆相クロマトグラフィーは、分離度が最も高いクロマトグラフィー技術であり、疎水性の高い条件下で動作します。しかし、HIC は中程度の疎水性条件下で動作します。 RPC と HIC は、疎水性に基づく 2 種類の分離技術です。 RPC と HIC の主な違いは、各手法で使用される疎水性の程度です。
参照:
1. 疎水性相互作用と逆相クロマトグラフィー:原理と方法 . GE ヘルスケア、2006 年。ここから入手可能
画像提供:
1.「逆相勾配溶出の概略図」Nategm 著 – Commons Wikimedia による自作 (CC BY-SA 4.0)
2. "Hicsalt" By Daliak at English Wikibooks – en.wikibooks から Commons に転送。 (パブリック ドメイン) コモンズ ウィキメディア経由